Positive og negative ioner:Hvordan metaller og ikke-metaller danner kationer og anioner
Af Carolyn LaRoche, Opdateret 24. marts 2022
Sinhyu/iStock/GettyImages
Hvad er en ion?
Atomer kan erhverve en elektrisk ladning ved enten at miste eller få elektroner og blive til ioner. En positivt ladet ion kaldes en kation , mens en negativt ladet ion er kendt som en anion . Ioner spiller en central rolle i ionbinding, som skaber mange af de forbindelser, vi møder dagligt.
Hvordan ioner dannes
Hvert atom indeholder protoner (positive), neutroner (neutrale) og elektroner (negative). Elektroner kredser om kernen og kan bevæge sig mellem atomer. Når et atom mister en eller flere elektroner, bliver det til en kation. Omvendt, når et atom får elektroner, bliver det en anion. Balancen mellem protoner og elektroner bestemmer ionens ladning.
Kationer:Positive ioner fra metaller
Metaller, som dominerer det periodiske system, mister let elektroner for at opnå en stabil elektronkonfiguration. De resulterende kationer bærer typisk en positiv ladning, der svarer til antallet af tabte elektroner. Ladningen varierer efter metallets gruppe:
- Gruppe 1-metaller (alkalimetaller) → +1
- Gruppe 2, 12 og 16 → +2
- Gruppe 13 og 15 → +3
- Gruppe 14 → +4
Fordi frie elektroner er rigelige i metaller, leder de elektricitet effektivt, en egenskab, der er direkte forbundet med kationdannelse.
Anioner:Negative ioner fra ikke-metaller
Ikke-metaller, placeret på højre side af det periodiske system, har en tendens til at få elektroner til at fylde deres valensskaller. Disse yderligere elektroner skaber et overskud af negativ ladning og danner anioner. De typiske ladninger afhænger af ikke-metallets gruppe:
- Gruppe 13 og 15 → –3
- Gruppe 14 → –4
- Gruppe 16 → –2
- Halogener (Gruppe 17) → –1
I modsætning til metaller leder ikke-metaller ikke elektricitet, fordi elektroner er tæt bundet til deres atomer.
Hvorfor dette betyder noget
Forståelse af iondannelse hjælper med at forklare en lang række kemiske fænomener - fra hvordan salt opløses i vand til hvordan biologiske celler opretholder elektriske gradienter. At genkende mønstret af ladninger på tværs af det periodiske system hjælper også med at forudsige grundstoffernes opførsel i kemiske reaktioner.
 Varme artikler
Varme artikler
-
 Havvand giver de første gram gulkage:Garnlignende materiale opsamler den største mængde uran til …Dette første gram gulkage blev fremstillet af uran fanget fra havvand med modificeret garn. Chien Wai og kolleger hos LCW Supercritical Technologies producerede den gule kage, en pulveriseret form for
Havvand giver de første gram gulkage:Garnlignende materiale opsamler den største mængde uran til …Dette første gram gulkage blev fremstillet af uran fanget fra havvand med modificeret garn. Chien Wai og kolleger hos LCW Supercritical Technologies producerede den gule kage, en pulveriseret form for -
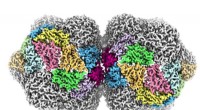 Ødelæggende plantevirus afsløres i atomiske detaljerBilledet viser strukturen af et geminivirus. Kredit:University of Leeds Den komplekse 3D-struktur af en af verdens mest dødelige familier af plantevira er blevet afsløret i enestående detaljer
Ødelæggende plantevirus afsløres i atomiske detaljerBilledet viser strukturen af et geminivirus. Kredit:University of Leeds Den komplekse 3D-struktur af en af verdens mest dødelige familier af plantevira er blevet afsløret i enestående detaljer -
 Beregning af varmeenergi i joule:en praktisk vejledningAf John Brennan, Opdateret 24. marts 2022 I begyndelsen af det 19. århundrede demonstrerede den britiske brygger og fysiker JamesJoule, at varme og mekanisk arbejde er to udtryk for den samme energi.
Beregning af varmeenergi i joule:en praktisk vejledningAf John Brennan, Opdateret 24. marts 2022 I begyndelsen af det 19. århundrede demonstrerede den britiske brygger og fysiker JamesJoule, at varme og mekanisk arbejde er to udtryk for den samme energi. -
 Ny struktur af nøgleprotein rummer spor for bedre lægemiddeldesignProber (vist glødende her) afslørede den indre arkitektur af proteinet A2aAR i den nye undersøgelse. Kredit:Kurt Wuthrich og Matthew Eddy, Scripps Research Institute Forskere ved The Scripps Resea
Ny struktur af nøgleprotein rummer spor for bedre lægemiddeldesignProber (vist glødende her) afslørede den indre arkitektur af proteinet A2aAR i den nye undersøgelse. Kredit:Kurt Wuthrich og Matthew Eddy, Scripps Research Institute Forskere ved The Scripps Resea
- Hvor er vulkanerne i Island placeret?
- Australien er ved at vedtage omfattende cyberlove på trods af teknologigigantens frygt
- Inside the man box:hvordan stive ideer om at bemande op skader unge mænd og dem omkring dem
- Hvordan videnskabsmænd bygger roterende maskiner med molekyler
- Isolering af kviksølv for at beskytte fødekæder
- Kan robotter være rådgivere? Tidlig forskning viser positiv brugeroplevelse


