Elektrolyse af vand:Forståelse af brint- og iltgasproduktion
* Vands kemiske formel: Vand (H2O) består af to hydrogenatomer (H) og et oxygenatom (O).
* Bræk bindingerne: Når elektricitet ledes gennem vand, giver det nok energi til at bryde de kemiske bindinger, der holder brint- og oxygenatomerne sammen.
* Gasdannelse: De frigjorte brintatomer binder sig sammen for at danne hydrogengas (H2), og oxygenatomerne binder sig for at danne oxygengas (O2).
Så afgives både brintgas og oxygengas under elektrolyse af vand.
Sidste artikelForståelse af N-H-bindingen:egenskaber og polaritet
Næste artikelIdentifikation af det manglende element i kulsyre (H2CO3)
 Varme artikler
Varme artikler
-
 En effektiv måde at fjerne atrazin og dets biprodukter i overfladevandKredit:Institut national de la recherche scientifique Atrazin, meget brugt som ukrudtsmiddel, er kendt for at have skadelige virkninger på akvatiske dyreliv og udgør en risiko for menneskers sundh
En effektiv måde at fjerne atrazin og dets biprodukter i overfladevandKredit:Institut national de la recherche scientifique Atrazin, meget brugt som ukrudtsmiddel, er kendt for at have skadelige virkninger på akvatiske dyreliv og udgør en risiko for menneskers sundh -
 Ingeniører er pionerer i platinskaldannelsesprocessen, opnå første observation nogensindeEn skal af platin vokser lag for lag under iltudglødning. Kredit:Pan Group / UCI UCI-forskere har udtænkt en ny metode til dynamisk at danne en platinskal på en nanopartikelkerne af metallisk lege
Ingeniører er pionerer i platinskaldannelsesprocessen, opnå første observation nogensindeEn skal af platin vokser lag for lag under iltudglødning. Kredit:Pan Group / UCI UCI-forskere har udtænkt en ny metode til dynamisk at danne en platinskal på en nanopartikelkerne af metallisk lege -
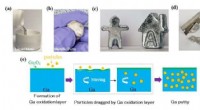 Spartellignende kompositter af galliummetal med potentiale til anvendelse i virkeligheden(a) Flydende gallium hældes i en beholder. (b) Galliumkitt støbes til en kugle. (c) Forskellige figurer fremstillet af galliumspartel. (d) Galliumspartel skæres af et blad. (e) Mekanismen for dannelse
Spartellignende kompositter af galliummetal med potentiale til anvendelse i virkeligheden(a) Flydende gallium hældes i en beholder. (b) Galliumkitt støbes til en kugle. (c) Forskellige figurer fremstillet af galliumspartel. (d) Galliumspartel skæres af et blad. (e) Mekanismen for dannelse -
 Stabilisering af emulsionsforskning forbedrer brandslukningsoperationer og mereKredit:Unsplash/CC0 Public Domain Forskere ved Texas A&M University har fundet en måde at kontrollere ladningen af nanopartikler på en to-væske grænseflade for at skabe et mere stabilt system, hv
Stabilisering af emulsionsforskning forbedrer brandslukningsoperationer og mereKredit:Unsplash/CC0 Public Domain Forskere ved Texas A&M University har fundet en måde at kontrollere ladningen af nanopartikler på en to-væske grænseflade for at skabe et mere stabilt system, hv
- Virksomheder har brug for en bedre tilgang til compliance-programmer, forskningsfund
- Ledning forekommer lettere mellem faste stoffer og væsker. Dette skyldes, at partiklerne i gasser e…
- Sådan foldes et lineært kromosom af Streptomyces
- Lufthansa aflyser Kina -flyvninger til slutningen af marts
- OCT-baseret teknik fanger subtile detaljer om fotoreceptorfunktion
- Hvor længe er et år på Planet Mars?


