Forståelse af N-H-bindingen:egenskaber og polaritet
* Kovalent binding: Nitrogen (N) og hydrogen (H) deler elektroner for at opnå en stabil elektronkonfiguration. Denne deling danner en kovalent binding.
* Polar: Nitrogen er mere elektronegativt end brint, hvilket betyder, at det tiltrækker de delte elektroner stærkere. Dette skaber en delvis negativ ladning (δ-) på nitrogenatomet og en delvis positiv ladning (δ+) på hydrogenatomet. Den ulige deling af elektroner gør bindingen polær.
Denne polaritet er vigtig, fordi den giver molekyler, der indeholder N-H-bindinger (som ammoniak, NH3) egenskaber som hydrogenbinding.
 Varme artikler
Varme artikler
-
 De skjulte risici i dine popcorn med smørsmag:Hvad videnskaben sigerEn filmaften derhjemme med en stor skål popcorn er et klassisk tidsfordriv, men snacken rummer mere end bare smag. Mens popcorn kan være en alsidig ingrediens – bruges som skorpe til stegt kylling, to
De skjulte risici i dine popcorn med smørsmag:Hvad videnskaben sigerEn filmaften derhjemme med en stor skål popcorn er et klassisk tidsfordriv, men snacken rummer mere end bare smag. Mens popcorn kan være en alsidig ingrediens – bruges som skorpe til stegt kylling, to -
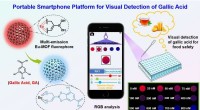 Ny fluorescenssensorplatform udviklet til visuel overvågning af fødevaresikkerhedDen bærbare smartphone-platform baseret på dual-emission Eu-MOF til visuel påvisning af gallussyre i fødevaresikkerheden. Kredit:Pan Lei Et forskerhold ledet af prof. Jiang Changlong fra Institute
Ny fluorescenssensorplatform udviklet til visuel overvågning af fødevaresikkerhedDen bærbare smartphone-platform baseret på dual-emission Eu-MOF til visuel påvisning af gallussyre i fødevaresikkerheden. Kredit:Pan Lei Et forskerhold ledet af prof. Jiang Changlong fra Institute -
 Fødevareforskere sigter mod at gøre plantebaseret protein smagere og sundereDavid Julian McClements er en fremtrædende professor i fødevarevidenskab ved UMass Amherst. Kredit:UMass Amherst I takt med at kødspisningen fortsætter med at stige rundt om i verden, fødevarefors
Fødevareforskere sigter mod at gøre plantebaseret protein smagere og sundereDavid Julian McClements er en fremtrædende professor i fødevarevidenskab ved UMass Amherst. Kredit:UMass Amherst I takt med at kødspisningen fortsætter med at stige rundt om i verden, fødevarefors -
 Nye materialer:En vippekontakt til katalyseEn perovskit tyndfilm elektrode, på en ZrO2-krystal. Kredit:TU Wien Elektrokemi spiller en stadig vigtigere rolle:Uanset om det er brændselsceller, elektrolyse eller kemisk energilagring, kemiske
Nye materialer:En vippekontakt til katalyseEn perovskit tyndfilm elektrode, på en ZrO2-krystal. Kredit:TU Wien Elektrokemi spiller en stadig vigtigere rolle:Uanset om det er brændselsceller, elektrolyse eller kemisk energilagring, kemiske
- Mere end 3, 300 Android -apps sporer børn forkert, undersøgelse finder
- Forskere rapporterer det første naturlige eksempel på et fossiliseret jordskælv i serpentinit
- Hvilket materiale ændrer sollys til kemisk energi?
- Hvordan coronavirus har fremhævet behovet for bedre transport i landdistrikterne
- Quo vadis Antarktis bundvand?
- 3D/4D-printede bio-piezoelektriske stilladser viser potentiale inden for knoglevævsteknik


