Densitetsændringer under faseovergange:fast, flydende og gas
Grundlæggende om tæthed
* Tæthed er et mål for, hvor meget masse der er pakket ind i et givet volumen. Det er beregnet som:
* Massefylde =masse/volumen
Faseændringer og tæthed
* Solid: I et fast stof er partikler tætpakket og vibrerer i faste positioner. Dette resulterer i den højeste tæthed af de tre faser. Tænk på en isblok – den er tæt og optager en bestemt mængde plads.
* Væske: I en væske er partikler stadig tæt på hinanden, men har mere frihed til at bevæge sig rundt. Det betyder, at de er lidt mindre tætte end faste stoffer. Forestil dig vand - det tager form af sin beholder, men er stadig relativt tæt.
* Gas: I en gas spredes partikler langt fra hinanden og bevæger sig frit. Dette resulterer i den laveste tæthed, fordi den samme masse er spredt over et meget større volumen. Tænk på luft – den er mindre tæt end vand eller is.
Nøglepunkter
* Tæthed falder med faseændring: Når et stof går fra fast til flydende til gas, falder dets massefylde generelt. Det skyldes, at partiklerne bliver mere spredt ud.
* Undtagelser: Der er nogle undtagelser fra denne regel, såsom vand. Vand er *mindre* tæt i sin faste tilstand (is) end i sin flydende tilstand. Denne usædvanlige adfærd skyldes den unikke hydrogenbinding i vandmolekyler.
Eksempel:Vand
1. Is (fast): Is er mindre tæt end flydende vand, hvorfor den flyder.
2. Vand (væske): Flydende vand har en højere densitet end is.
3. Vanddamp (gas): Vanddamp er den mindst tætte af de tre.
Opsummering: Massefylde er en nøgleegenskab, der ændrer sig forudsigeligt, efterhånden som stoffer ændrer faser. Det er et koncept, der hjælper os med at forstå stoffets adfærd i forskellige former.
 Varme artikler
Varme artikler
-
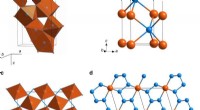 Forskere skaber umulige materialer på en enkel mådeKrystalstrukturer af jern-nitrogenforbindelser. Orange og blå kugler viser positionerne af Fe- og N -atomer, henholdsvis. (a) Fe3N2 ved 50? GPa. Strukturen er bygget af firkantede trigonale prismer NF
Forskere skaber umulige materialer på en enkel mådeKrystalstrukturer af jern-nitrogenforbindelser. Orange og blå kugler viser positionerne af Fe- og N -atomer, henholdsvis. (a) Fe3N2 ved 50? GPa. Strukturen er bygget af firkantede trigonale prismer NF -
 Beregn fryse- og kogepunkter for opløsninger:Trin-for-trin-vejledningAf Timothy Banas • Opdateret 24. marts 2022 Mens frysepunktet (0°C) og kogepunktet (100°C) for rent vand er almindelig kendt, ændrer tilsætning af et opløst stof disse temperaturer. Salt i vand sænke
Beregn fryse- og kogepunkter for opløsninger:Trin-for-trin-vejledningAf Timothy Banas • Opdateret 24. marts 2022 Mens frysepunktet (0°C) og kogepunktet (100°C) for rent vand er almindelig kendt, ændrer tilsætning af et opløst stof disse temperaturer. Salt i vand sænke -
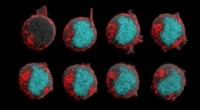 Forskere viser, at en kræftforsvarsmekanisme kan vendes tilbage for at angribe tumorerI disse time-lapse billeder, kimære antigenreceptorer reagerer på et opløseligt cytokin, udløser T-celleaktivering. Kredit:ZeNan Chang og Michael Lorenzini UCLA ingeniører og videnskabsmænd har ko
Forskere viser, at en kræftforsvarsmekanisme kan vendes tilbage for at angribe tumorerI disse time-lapse billeder, kimære antigenreceptorer reagerer på et opløseligt cytokin, udløser T-celleaktivering. Kredit:ZeNan Chang og Michael Lorenzini UCLA ingeniører og videnskabsmænd har ko -
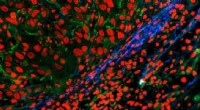 Oplyser vævsdannelse gennem flourescensBillede af tumorgrænse taget ved hjælp af fluorescensmikroskopi. Det nye markørmolekyle viser grænsen for tumoren i blåt; tumorvævet kan ses over det til venstre. Grøn:kollagen, rød:cellekerner. Kredi
Oplyser vævsdannelse gennem flourescensBillede af tumorgrænse taget ved hjælp af fluorescensmikroskopi. Det nye markørmolekyle viser grænsen for tumoren i blåt; tumorvævet kan ses over det til venstre. Grøn:kollagen, rød:cellekerner. Kredi
- Et stof, hvis form let kan ændre sig, er en?
- Bombardier til at skære 5, 000 job i omstrukturering
- Robotgribere i Spider-Man-stil trodser tyngdekraften
- Fremstilling af fejlfri grafenbelægninger
- Hvad består klorblegemiddel af?
- Fangst ekstracellulære vesikler:En ny teknologi til isolering af sygdomsmarkører


