Brintforbrænding:Oxidation, bindingsdannelse og vandproduktion
Reaktionen:
2 H2 (g) + O2 (g) → 2 H2O (l)
Oxidation:
* Brint (H₂) oxideres. Oxidation er tab af elektroner. I denne reaktion mister hvert brintatom en elektron for at blive en hydrogenion (H⁺).
Obligationsdannelse:
* Der dannes kovalente bindinger. Vand (H2O) dannes ved deling af elektroner mellem brint- og oxygenatomer. Hvert oxygenatom deler to elektroner med to brintatomer og danner to kovalente bindinger.
Forklaring:
1. Reaktanter: Gasformigt brint (H2) og gasformigt oxygen (O2) er udgangsmaterialerne.
2. Forbrænding: Når brint brænder, reagerer det hurtigt med ilt og frigiver energi i form af varme og lys.
3. Elektronoverførsel: Hydrogenatomer, som har en lavere elektronegativitet end oxygen, mister elektroner og bliver positivt ladet (H⁺). Iltatomer får disse elektroner og bliver negativt ladede (O²⁻).
4. Vanddannelse: De positivt ladede hydrogenioner (H⁺) og negativt ladede oxygenioner (O²⁻) tiltrækker hinanden og danner kovalente bindinger, hvilket skaber vandmolekyler (H₂O).
Oversigt:
* Oxideret molekyle: Brint (H₂)
* Bindelse dannet: Kovalente bindinger i vandmolekylet (H2O)
 Varme artikler
Varme artikler
-
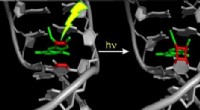 Belysning af reaktionsmekanismen ved PUVA-lysterapi til hudsygdommeReaktionsstadier, når et psoralenmolekyle binder til DNA. Resultatet er, at psoralen er permanent bundet til DNAet via en cyclobutanring. Cellen er ændret og dermed beskadiget, og udløser processen me
Belysning af reaktionsmekanismen ved PUVA-lysterapi til hudsygdommeReaktionsstadier, når et psoralenmolekyle binder til DNA. Resultatet er, at psoralen er permanent bundet til DNAet via en cyclobutanring. Cellen er ændret og dermed beskadiget, og udløser processen me -
 Digital penicillinproduktionBioreaktor ved TU Wien. Kredit:Vienna University of Technology TU Wien og Sandoz GmbH har med succes implementeret en computersimulering i realtid af penicillinproducerende organismers komplekse v
Digital penicillinproduktionBioreaktor ved TU Wien. Kredit:Vienna University of Technology TU Wien og Sandoz GmbH har med succes implementeret en computersimulering i realtid af penicillinproducerende organismers komplekse v -
 Menneskelige farer hæmmer forskning i vampyrflagermusgiftKredit:University of Queensland Vampyrflagermus kan holde nøglen til nye behandlinger for en række alvorlige medicinske problemer, men forskere har ramt en hage ved at få adgang til de prøver, der
Menneskelige farer hæmmer forskning i vampyrflagermusgiftKredit:University of Queensland Vampyrflagermus kan holde nøglen til nye behandlinger for en række alvorlige medicinske problemer, men forskere har ramt en hage ved at få adgang til de prøver, der -
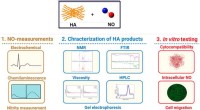 Forskere bruger nitrogenoxidopfangere til at målrette mod triple-negativ brystkræftBiomakromolekyler DOI:10.1021/acs.biomac.2c00545 Forskere udforsker en potentiel ny terapeutisk tilgang til tredobbelt negativ brystkræftbehandling. Amir Abdo Alsharabasy, en CÚRAM ph.d.-kandidat,
Forskere bruger nitrogenoxidopfangere til at målrette mod triple-negativ brystkræftBiomakromolekyler DOI:10.1021/acs.biomac.2c00545 Forskere udforsker en potentiel ny terapeutisk tilgang til tredobbelt negativ brystkræftbehandling. Amir Abdo Alsharabasy, en CÚRAM ph.d.-kandidat,
- Krop, hvis store størrelse tiltrækker andre genstande gennem tyngdekraften?
- Hvor mange luftmasser er involveret i en stationær front?
- Nyt katodedesign løser stor barriere for bedre lithium-ion-batterier
- Undersøgelse kaster lys over nye IEEE-standardkategorier, viser effekt på elsystemet
- Hvad er en abiotisk faktor i et økosystem?
- Undersøgelse:Vælgerne vil have kandidater, parter til at handle på klimaforandringer


