Azoxymethan (AZOXYMETHAne) Lewis-struktur:En trin-for-trin guide
Sådan tegner du dens Lewis-struktur:
1. Tæl valenselektroner:
* Kulstof (C):4 valenselektroner
* Brint (H):1 valenselektron (x3)
* Nitrogen (N):5 valenselektroner (x2)
* Ilt (O):6 valenselektroner (x2)
Samlede valenselektroner =4 + 3 + 10 + 12 =29
2. Bestem det centrale atom:
Nitrogen er normalt det centrale atom i forbindelser, der indeholder N-N-bindinger.
3. Tegn et grundlæggende skelet:
Den grundlæggende struktur af Azoxymethan kan repræsenteres som:
```
H
|
H - C - N =N - O - O
|
H
```
4. Placer bindingselektroner:
Forbind alle atomer med enkeltbindinger ved at bruge 8 elektroner til enkeltbindingerne:
```
H
|
H - C - N =N - O - O
|
H
```
5. Fordel resterende elektroner:
Vi har brugt 8 elektroner, hvilket efterlader 21 elektroner at fordele.
* Placer 6 elektroner omkring hvert iltatom for at fuldende deres oktetter.
* Placer 2 elektroner omkring hvert brintatom for at fuldende deres duet.
* Placer de resterende 5 elektroner som enlige par på nitrogenatomerne.
6. Overvej en formel opkrævning:
For at sikre den mest stabile Lewis-struktur skal du kontrollere den formelle ladning på hvert atom. Den formelle ladning af et atom beregnes som:
Formel ladning =(Valenselektroner) - (Ikke-bindende elektroner) - (1/2 Bindingselektroner)
* Kulstof:4 - 0 - 4 =0
* Brint:1 - 0 - 1 =0
* Nitrogen (venstre):5 - 2 - 4 =-1
* Nitrogen (højre):5 - 4 - 3 =0
* Ilt (venstre):6 - 6 - 1 =-1
* Ilt (højre):6 - 6 - 1 =-1
7. Endelig Lewis-struktur:
```
H
|
H - C - N =N - O - O
|
H
....
/\/\
:N ::O :O
| |
-1 -1
```
Denne struktur opfylder oktetreglen for alle atomer undtagen nitrogenet til venstre, som har 7 elektroner. Dette er dog en almindelig forekomst i nitrogenholdige forbindelser, og strukturen anses stadig for gyldig.
Husk, at Lewis-strukturer kun er en repræsentation af binding og ikke er beregnet til at være en nøjagtig afbildning af molekylet.
 Varme artikler
Varme artikler
-
 Bioaktive naturlige forbindelser til kampen mod kræftSojaplanter producerer glyceolliner som reaktion på patogenangreb såsom svampe, bakterier eller UV-bestråling, for at bevare deres helbred. Kredit:pixabay.com Phytoalexiner er bioaktive fytokemika
Bioaktive naturlige forbindelser til kampen mod kræftSojaplanter producerer glyceolliner som reaktion på patogenangreb såsom svampe, bakterier eller UV-bestråling, for at bevare deres helbred. Kredit:pixabay.com Phytoalexiner er bioaktive fytokemika -
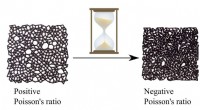 Brug af en materialehukommelse til at kode unikke fysiske egenskaberForskere har vist, at et materiales naturlige ældningsproces kan udnyttes til at skabe materialer med usædvanlige egenskaber. Kredit:Nidhi Pashine En ny undersøgelse offentliggjort i Videnskabens
Brug af en materialehukommelse til at kode unikke fysiske egenskaberForskere har vist, at et materiales naturlige ældningsproces kan udnyttes til at skabe materialer med usædvanlige egenskaber. Kredit:Nidhi Pashine En ny undersøgelse offentliggjort i Videnskabens -
 Gennembrudende retsmedicinsk tilgang til at hjælpe med at slå ned på salget af falske stofferKredit:CC0 Public Domain Falske lægemidler er et af de største sundhedsproblemer i verden i dag. Den internationale kriminalpolitiorganisation (INTERPOL) oplevede en stigning i falske medicinske
Gennembrudende retsmedicinsk tilgang til at hjælpe med at slå ned på salget af falske stofferKredit:CC0 Public Domain Falske lægemidler er et af de største sundhedsproblemer i verden i dag. Den internationale kriminalpolitiorganisation (INTERPOL) oplevede en stigning i falske medicinske -
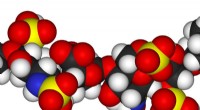 Den tid, der er nødvendig for at sekvensere nøglemolekyler, kan reduceres fra år til minutterEn nanopore og billedgenkendelsessoftware kan sekvensere en sulfateret glycosaminoglycan i realtid. Kredit:Rensselaer Polytekniske Institut Ved at bruge en nanopore, forskere har demonstreret pote
Den tid, der er nødvendig for at sekvensere nøglemolekyler, kan reduceres fra år til minutterEn nanopore og billedgenkendelsessoftware kan sekvensere en sulfateret glycosaminoglycan i realtid. Kredit:Rensselaer Polytekniske Institut Ved at bruge en nanopore, forskere har demonstreret pote
- Hvad er forskellen mellem fluvial og alluvial jord?
- Hvad er det udtryk, der bruges til at beskrive, når Magma stiger overfladen, men ikke forekommer ve…
- Hvordan man beregner mol af produkter produceret i et laboratorieeksperiment
- Hvad er fysikens funktion?
- Celleorganeller:eksempler og opdelte funktioner
- Hvilken slags træer mister deres blade om efteråret?


