Guld- og platinreaktivitet:Forståelse af ædelmetalegenskaber
* Placering: De er begge placeret i overgangsmetalgruppen, specifikt i "møntmetallerne" (gruppe 11). Denne gruppe er kendt for sin lave reaktivitet sammenlignet med andre overgangsmetaller.
* Ædelmetaller: Guld og platin betragtes som "ædelmetaller" på grund af deres modstandsdygtighed over for oxidation og korrosion. Dette betyder, at de ikke let reagerer med ilt eller andre almindelige elementer i miljøet.
* Høj ioniseringsenergi: Guld og platin har høje ioniseringsenergier, hvilket betyder, at det kræver meget energi at fjerne en elektron fra deres atomer. Dette bidrager til deres modstandsdygtighed over for kemiske reaktioner.
* Brug i smykker: Deres træghed gør dem ideelle til smykker, hvor de bevarer deres glans og udseende over lange perioder.
Der er dog nogle vigtige punkter at overveje:
* Ikke helt inaktivt: Selvom de er meget ureaktive, kan de stadig reagere under specifikke forhold. For eksempel kan de opløses i aqua regia (en blanding af salpetersyre og saltsyre) eller reagere med halogener (som klor) ved høje temperaturer.
* Katalytisk aktivitet: Begge metaller kan bruges som katalysatorer i forskellige kemiske reaktioner, hvilket viser, at de kan deltage i kemiske processer under specifikke forhold.
Som konklusion, mens guld og platin er blandt de mindst reaktive metaller, er de ikke helt inerte. Deres specifikke reaktivitet afhænger af det kemiske miljø og tilstedeværelsen af specifikke reagenser.
 Varme artikler
Varme artikler
-
 Særligt blåt lys – forsker finder ud af, at nye kemiske klynger udsender meget effektivt lysKredit:Wiley Et forskningshold fra Florida State University har opdaget, at en unik organisk-uorganisk forbindelse, der indeholder nul-dimensionelle molekylære klynger, udsender et meget effektivt
Særligt blåt lys – forsker finder ud af, at nye kemiske klynger udsender meget effektivt lysKredit:Wiley Et forskningshold fra Florida State University har opdaget, at en unik organisk-uorganisk forbindelse, der indeholder nul-dimensionelle molekylære klynger, udsender et meget effektivt -
 Vil dit fremtidige tøj være lavet af alger?En mini-T-shirt demonstrerer de fotosyntetiske levende materialer skabt i laboratoriet af University Rochester biolog Anne S. Meyer og Delft University of Technology bionanoforsker Marie-Eve Aubin-Tam
Vil dit fremtidige tøj være lavet af alger?En mini-T-shirt demonstrerer de fotosyntetiske levende materialer skabt i laboratoriet af University Rochester biolog Anne S. Meyer og Delft University of Technology bionanoforsker Marie-Eve Aubin-Tam -
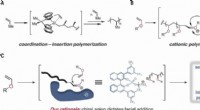 Brug af en organokatalysator til at stereokontrollere polymerisationDesign af en stereoselektiv kationisk polymerisation. (A) Det chirale ligandmiljø i koordinations-insertion-polymerisationer muliggør stereoselektiv monomer-enchainment ved at dirigere ansigtsaddition
Brug af en organokatalysator til at stereokontrollere polymerisationDesign af en stereoselektiv kationisk polymerisation. (A) Det chirale ligandmiljø i koordinations-insertion-polymerisationer muliggør stereoselektiv monomer-enchainment ved at dirigere ansigtsaddition -
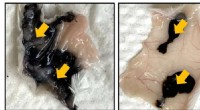 En forbedret blæk til kolontatoveringerEt kommercielt blæk (venstre) diffunderer langt fra injektionssteder (pile) under musens hud, men et nyt kolontatoveringsblæk (højre) diffunderer meget mindre. Kredit:Jordan Yaron, Ph.D. Tyktarmen
En forbedret blæk til kolontatoveringerEt kommercielt blæk (venstre) diffunderer langt fra injektionssteder (pile) under musens hud, men et nyt kolontatoveringsblæk (højre) diffunderer meget mindre. Kredit:Jordan Yaron, Ph.D. Tyktarmen


