Lithiums reaktivitet med vand:Hvorfor mindre kraftig end natrium og kalium?
1. Mindre størrelse og højere ioniseringsenergi:
* Lithium er det mindste alkalimetal, hvilket fører til en højere koncentration af positiv ladning på dets enkelte ydre elektron. Denne stærke tiltrækning mellem kernen og dens ydre elektron resulterer i en højere ioniseringsenergi, hvilket betyder, at det tager mere energi at fjerne den elektron.
* Denne højere ioniseringsenergi gør det mindre sandsynligt for lithium at donere sin elektron til vandmolekyler, hvilket er et afgørende trin i reaktionen.
2. Hydration Entalpi:
* Mens lithium har en mindre størrelse, er dets hydreringsentalpi (den energi, der frigives, når ioner hydreres af vandmolekyler) betydeligt højere end natrium og kalium.
* Denne høje hydreringsentalpi hjælper med at stabilisere lithiumioner i opløsning og reducerer yderligere drivkraften for reaktionen.
3. Overfladeareal:
* Lithium har i sin faste form et meget mindre overfladeareal sammenlignet med natrium og kalium. Dette reducerer kontaktområdet mellem lithium og vand, hvilket begrænser reaktionshastigheden.
4. Dannelse af et beskyttende lag:
* Når lithium reagerer med vand, danner det et tyndt lag lithiumhydroxid (LiOH) på overfladen. Dette lag fungerer som en barriere, der hindrer yderligere reaktion med vand.
Samlet set:
Disse faktorer bidrager til lithiums mindre kraftige reaktion med vand sammenlignet med natrium og kalium. Mens den reagerer, er reaktionen langsommere og mindre eksplosiv på grund af dens mindre størrelse, højere ioniseringsenergi, høj hydreringsentalpi og dannelsen af et beskyttende lag.
Sidste artikelBrint og ilts vitale rolle i cellulær funktion
Næste artikelKovalente bindinger i frugt:Forståelse af kemisk sammensætning
 Varme artikler
Varme artikler
-
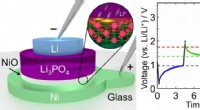 Lille, hurtig, og meget energieffektiv hukommelsesenhed inspireret af lithium-ion-batterierDe stablede lag i den foreslåede hukommelsesenhed danner et minibatteri, der hurtigt og effektivt kan skiftes mellem tre forskellige spændingstilstande (0,95 V, 1,35 V, og 1,80 V). Kredit:ACS Applied
Lille, hurtig, og meget energieffektiv hukommelsesenhed inspireret af lithium-ion-batterierDe stablede lag i den foreslåede hukommelsesenhed danner et minibatteri, der hurtigt og effektivt kan skiftes mellem tre forskellige spændingstilstande (0,95 V, 1,35 V, og 1,80 V). Kredit:ACS Applied -
 Nyt proteinstudie udvider kendskabet til molekylært grundlag for sygdomPatricia Clark, pastor John Cardinal OHara C.S.C. Professor i kemi og biokemi ved Notre Dame, arbejdede sammen med Tobin Sosnick, professor og formand for Institut for Biokemi og Molekylærbiologi ved
Nyt proteinstudie udvider kendskabet til molekylært grundlag for sygdomPatricia Clark, pastor John Cardinal OHara C.S.C. Professor i kemi og biokemi ved Notre Dame, arbejdede sammen med Tobin Sosnick, professor og formand for Institut for Biokemi og Molekylærbiologi ved -
 At fange atomer i aktion:se næste generations materialer krystallisereEn af de mange mulige ruter til næste generations materialer-dem, der muliggør nye fremskridt inden for datalagring, elektroniske anordninger, og lettere og stærkere strukturelle byggematerialer - er
At fange atomer i aktion:se næste generations materialer krystallisereEn af de mange mulige ruter til næste generations materialer-dem, der muliggør nye fremskridt inden for datalagring, elektroniske anordninger, og lettere og stærkere strukturelle byggematerialer - er -
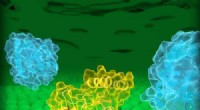 Forskere rapporterer den første 3D-struktur af DHHC-enzymerHuman DHHC20 (gul) er indlejret i Golgi-membranen (grøn), et rum placeret inde i celler. DHHC20 knytter en fedtsyrekæde (hvid) til et målprotein (blå, forgrund), som forankrer proteinet til Golgi-memb
Forskere rapporterer den første 3D-struktur af DHHC-enzymerHuman DHHC20 (gul) er indlejret i Golgi-membranen (grøn), et rum placeret inde i celler. DHHC20 knytter en fedtsyrekæde (hvid) til et målprotein (blå, forgrund), som forankrer proteinet til Golgi-memb
- Udforsk ametystens betydning:Opdag dens helbredende egenskaber og anvendelser
- Atmosfæriske metallag vises med overraskende regelmæssighed
- De første videoer nogensinde viser, hvordan varme bevæger sig gennem materialer på nanoskalaen og…
- Hvordan man ved, om et element har en positiv eller negativ ladning
- Hvad er komprimerbar det en gasvæske eller fast?
- Robot 3-D udskriver erstatningsbeslag på forlygten


