Dekomponering og syntesereaktioner:Definitioner og eksempler
Dekomponering og syntese:modsatrettede kemiske reaktioner
Dekomponering og syntese er to grundlæggende begreber i kemi, der beskriver modsatte kemiske processer:
Dekomponering:
* Definition: En kemisk reaktion, hvor en enkelt reaktant nedbrydes til to eller flere enklere produkter.
* Eksempel: Nedbrydningen af hydrogenperoxid (H2O2) til vand (H2O) og oxygengas (O2).
* 2 H202 -> 2 H20 + O2
* Karakteristika:
* Kræver normalt energitilførsel (varme, lys, elektricitet).
* Skaber enklere stoffer ud fra et komplekst.
* Indebærer ofte at bryde bånd.
Syntese:
* Definition: En kemisk reaktion, hvor to eller flere reaktanter kombineres for at danne et enkelt, mere komplekst produkt.
* Eksempel: Dannelse af vand fra brint og ilt.
* 2 H2 + O2 -> 2 H20
* Karakteristika:
* Frigiver ofte energi (eksotermisk).
* Skaber et mere komplekst stof fra simplere.
* Indebærer normalt dannelse af nye bindinger.
Tænk på det som at bygge med LEGO'er:
* Dekomponering: Nedbrydning af en kompleks LEGO-struktur i mindre stykker.
* Syntese: Opbygning af en kompleks struktur fra mindre LEGO-stykker.
Opsummering:
Nedbrydning er som at skille ting ad, mens syntese er som at sætte ting sammen. De er modsatte processer, der er afgørende for at forstå, hvordan kemiske reaktioner fungerer.
Ud over kemi:
Begreberne nedbrydning og syntese kan anvendes på forskellige områder, som:
* Biologi: Nedbrydning af organisk stof af bakterier og svampe, syntese af proteiner og kulhydrater af levende organismer.
* Musik: Dekomponering af en kompleks melodi til individuelle toner, syntese af en ny melodi fra individuelle toner.
* Kunst: Dekomponering af et billede i dets grundlæggende elementer, syntese af et nyt billede fra disse elementer.
Disse termer bruges til at beskrive en bred vifte af processer, der involverer nedbrydning og konstruktion af ting.
 Varme artikler
Varme artikler
-
 Sådan kombineres kemiske ligninger:En trin-for-trin guideAf Sean Lancaster Opdateret 30. august 2022 AlexRaths/iStock/GettyImages Kemiske ligninger er kemiens sprog - de beskriver, hvordan stoffer transformeres under en reaktion. For ligetil transformati
Sådan kombineres kemiske ligninger:En trin-for-trin guideAf Sean Lancaster Opdateret 30. august 2022 AlexRaths/iStock/GettyImages Kemiske ligninger er kemiens sprog - de beskriver, hvordan stoffer transformeres under en reaktion. For ligetil transformati -
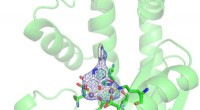 Fremskridt mod en ny influenzabehandling, takket være en lille justeringEt nyt antiviralt lægemiddel hæmmer replikation af influenzas genom ved at binde sig til manganioner (lilla kugler). Kredit:Christine Morrison Dette års uventet aggressive influenzasæson minder al
Fremskridt mod en ny influenzabehandling, takket være en lille justeringEt nyt antiviralt lægemiddel hæmmer replikation af influenzas genom ved at binde sig til manganioner (lilla kugler). Kredit:Christine Morrison Dette års uventet aggressive influenzasæson minder al -
 Et nyt potentielt alternativ til myggebekæmpelse opdagetKredit:CC0 Public Domain Naturlige æteriske olier udvundet af skallen af en citrusfrugt kunne være et effektivt nyt miljøvenligt alternativ i myggekontrolprogrammer, rapporterer en ny undersøgel
Et nyt potentielt alternativ til myggebekæmpelse opdagetKredit:CC0 Public Domain Naturlige æteriske olier udvundet af skallen af en citrusfrugt kunne være et effektivt nyt miljøvenligt alternativ i myggekontrolprogrammer, rapporterer en ny undersøgel -
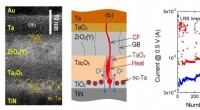 En optimeret struktur af memristiv enhed til neuromorfe computersystemerHøjopløselig transmissionselektronmikroskopibillede (a) og skematisk (b) af tværsnittet af flerlags memristive strukturen i området for den ledende filament (CF), afhængigheden af resistive tilstand
En optimeret struktur af memristiv enhed til neuromorfe computersystemerHøjopløselig transmissionselektronmikroskopibillede (a) og skematisk (b) af tværsnittet af flerlags memristive strukturen i området for den ledende filament (CF), afhængigheden af resistive tilstand
- Hvornår er det bedste tidspunkt at se blodmåne?
- Er Jorden i brand? Data viser næsten fem gange så mange brande i sidste år
- Forskere opdager nøglen til molekylært mysterium om, hvordan planter reagerer på skiftende forhol…
- Klimateknik skal se på det store billede, siger forsker
- Nedbrydningsreaktioner:Nedbrydning af kemikalier forklaret
- Ørkenplanterodsystemer:Tilpasning til tørre miljøer


