Elektrolyse af saltlage:Forståelse af anodereaktioner (klorid vs. hydroxid)
Faktorer, der påvirker udledning:
* Elektrodepotentiale: Den lethed, hvormed en ion aflades, afhænger af dens standardelektrodepotentiale (E°). Chloridioner har et mere positivt standardelektrodepotentiale end hydroxidioner. Dette betyder, at chloridioner lettere oxideres (taber elektroner) ved anoden.
* Koncentration: Koncentrationen af ioner i opløsningen spiller også en rolle. I en saltvandsopløsning er koncentrationen af chloridioner væsentligt højere end hydroxidioners.
* Overpotentiale: Det faktiske potentiale, der kræves for at en reaktion kan forekomme, er ofte højere end standardelektrodepotentialet på grund af overpotentialet. Dette er en modstand mod reaktionen, der forekommer på elektrodeoverfladen. Men i dette tilfælde er overpotentialet for chloridoxidation lavere end for hydroxidoxidation.
Reaktionen ved anoden:
Ved anoden oxideres chloridionerne til klorgas:
2Cl- (vandig) → Cl2(g) + 2e-
Hvorfor udleder hydroxidioner ikke:
Hydroxidioner har et mere negativt standardelektrodepotentiale, hvilket gør dem mindre tilbøjelige til at blive oxideret. Derudover betyder tilstedeværelsen af en stor koncentration af chloridioner, at de er lettere tilgængelige for reaktion ved anoden.
Oversigt:
Ved elektrolyse af saltlage gør kombinationen af et mere positivt standardelektrodepotentiale, højere koncentration og lavere overpotentiale for chloridioner dem til den foretrukne art, der skal aflades ved anoden. Dette resulterer i produktion af klorgas.
 Varme artikler
Varme artikler
-
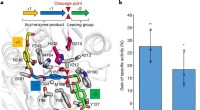 Konstrueret enzym i stand til at nedbryde PET på ti timeren, Strukturel model af 2-HE (MHET) 3 (farvet pindmodel) forankret i vildtype LCC (gråt bånd). Det formodede substratbindingssted for LCC kan opdeles i tre undersider (-2, −1, +1), hver i kontakt med
Konstrueret enzym i stand til at nedbryde PET på ti timeren, Strukturel model af 2-HE (MHET) 3 (farvet pindmodel) forankret i vildtype LCC (gråt bånd). Det formodede substratbindingssted for LCC kan opdeles i tre undersider (-2, −1, +1), hver i kontakt med -
 Hamp testlaboratorium lanceret som svar på industriens behovChristopher Perkins 89 (CAHNR) 95 MS, anbringer bakker med hamp i en tørremaskine på UConns Center for Environmental Sciences and Engineering laboratorium. Kredit:Sean Flynn/UConn Som svar på en h
Hamp testlaboratorium lanceret som svar på industriens behovChristopher Perkins 89 (CAHNR) 95 MS, anbringer bakker med hamp i en tørremaskine på UConns Center for Environmental Sciences and Engineering laboratorium. Kredit:Sean Flynn/UConn Som svar på en h -
 Teknologi fremskynder processen med at opdage salmonella, E coli, andre fødevarebårne sygdommeEn prisvindende Purdue University-teknologi bruger en biochip til at indsamle og analysere mikrober i madprøver og fremskynde processen med at opdage fødevarebårne sygdomme. Kredit:Michael Ladisch
Teknologi fremskynder processen med at opdage salmonella, E coli, andre fødevarebårne sygdommeEn prisvindende Purdue University-teknologi bruger en biochip til at indsamle og analysere mikrober i madprøver og fremskynde processen med at opdage fødevarebårne sygdomme. Kredit:Michael Ladisch -
 En stabil kobberkatalysator til omdannelse af kuldioxidKredit:CC0 Public Domain En ny katalysator til omdannelse af kuldioxid (CO 2 ) til kemikalier eller brændstoffer er blevet udviklet af forskere ved Ruhr-Universität Bochum og University of Duisb
En stabil kobberkatalysator til omdannelse af kuldioxidKredit:CC0 Public Domain En ny katalysator til omdannelse af kuldioxid (CO 2 ) til kemikalier eller brændstoffer er blevet udviklet af forskere ved Ruhr-Universität Bochum og University of Duisb
- Ny undersøgelse afslører, hvordan parasitter former komplekse fødevæv
- Hvorfor kaldes Europa en satellit og ikke planet?
- Sådan beregnes Toroidal Transformers
- Hvad bruges gassen kuldioxid til?
- MH370 burde få os til at genoverveje, hvordan vi overvåger fly
- Hvornår opdagede Alfred Wegener teorien om pladetektonik?


