Sublimering i kemi:definition, proces og eksempler
Her er en oversigt:
* Solid: Et stof i sin faste tilstand har molekyler tæt pakket sammen i en fast struktur.
* Gas: I en gasform er molekyler vidt fordelt og bevæger sig frit.
* Sublimering: Processen med at springe den flydende fase helt over og gå direkte fra fast til gas.
Eksempler på sublimering:
* Tøris: Fast kuldioxid (CO2) sublimerer ved stuetemperatur og -tryk og danner en kold, tæt gas.
* Naphthalen: Mølkugler er lavet af naphthalen, som sublimerer langsomt og frigiver en damp, der afviser møl.
* Frysetørring: Denne teknik bruger sublimering til at fjerne vand fra maden og bevare det uden at beskadige dets næringsstoffer.
Faktorer, der påvirker sublimering:
* Temperatur: Højere temperaturer øger molekylernes energi, hvilket gør sublimering mere sandsynlig.
* Tryk: Lavere tryk tillader molekyler at undslippe den faste fase lettere, hvilket fremmer sublimering.
* Intermolekylære kræfter: Stoffer med svage intermolekylære kræfter er mere tilbøjelige til at sublimere.
Forskel mellem sublimering og fordampning:
Mens begge involverer overgange fra en kondenseret fase til en gas, adskiller de sig i startfasen:
* Sublimering: Fast → Gas
* Fordampning: Væske → Gas
Sig til, hvis du har andre spørgsmål!
Sidste artikelForstå væsketyper:vand, olie og kviksølv - kemiske egenskaber
Næste artikelForståelse af pH:Er en pH på 3 sur?
 Varme artikler
Varme artikler
-
 Forskere optrævler hemmelighederne om, hvordan natursten lyser i mørkeGlow-in-the-mørke hackmanit. Kredit:Mika Lastusaari Forskere ved Universitetet i Turku, Finland, har opdaget oprindelsen af gløden i det naturlige mineral, der genererer hvid luminescens i mørke
Forskere optrævler hemmelighederne om, hvordan natursten lyser i mørkeGlow-in-the-mørke hackmanit. Kredit:Mika Lastusaari Forskere ved Universitetet i Turku, Finland, har opdaget oprindelsen af gløden i det naturlige mineral, der genererer hvid luminescens i mørke -
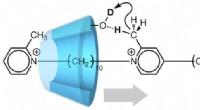 Molekylær maskine udnytter bevægelse i en enkelt retningFig.1. En pseudo-rotaxan (kunstig molekylær maskine), hvor translationel bevægelse af α-cyclodextrin (α-CD) falder sammen med deuteration. Når α-CD bevæger sig langs to-stationsaksemolekylet som vist
Molekylær maskine udnytter bevægelse i en enkelt retningFig.1. En pseudo-rotaxan (kunstig molekylær maskine), hvor translationel bevægelse af α-cyclodextrin (α-CD) falder sammen med deuteration. Når α-CD bevæger sig langs to-stationsaksemolekylet som vist -
 Forskere opfinder processen til fremstilling af bæredygtigt gummi, plastikVores team kombinerede en katalysator, vi for nylig har opdaget, med ny og spændende kemi for at finde det første høje udbytte, lavprismetode til fremstilling af butadien, siger Dionisios Vlachos, Dir
Forskere opfinder processen til fremstilling af bæredygtigt gummi, plastikVores team kombinerede en katalysator, vi for nylig har opdaget, med ny og spændende kemi for at finde det første høje udbytte, lavprismetode til fremstilling af butadien, siger Dionisios Vlachos, Dir -
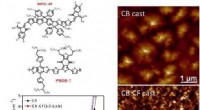 Binær opløsningsmiddelblanding, der øger høj effektivitet af polymersolcellerDe kemiske strukturer af elektrondonor PBDB-T og fluoreret NFA INPIC-4F; J-V karakteristika for PBDB-T:INPIC-4F solceller støbt af forskellige opløsningsmidler; AFM-billederne af PBDB-T:INPIC-4F overf
Binær opløsningsmiddelblanding, der øger høj effektivitet af polymersolcellerDe kemiske strukturer af elektrondonor PBDB-T og fluoreret NFA INPIC-4F; J-V karakteristika for PBDB-T:INPIC-4F solceller støbt af forskellige opløsningsmidler; AFM-billederne af PBDB-T:INPIC-4F overf
- EU rykker mod chipproducenten Broadcom i den seneste amerikanske teknologisalve
- Hvordan genererer Vattenfall elektricitet?
- Hvis det arbejde, der udføres på et objekt, fordobler sin kinetiske energi, dobbelthastigheden?
- Forskere viser, at langsomtgående jordskælv styres af stenpermeabilitet
- Sådan fungerer Jet Lag
- Fare for åndedrætsolie Smoke


