Forstå baser:forbindelser, der producerer hydroxidioner
Her er nogle eksempler:
* Metalhydroxider: Disse er den mest almindelige type baser. De har den generelle formel M(OH)n, hvor M er et metal, og n er antallet af hydroxidioner. For eksempel er natriumhydroxid (NaOH), kaliumhydroxid (KOH) og calciumhydroxid (Ca(OH)2) alle stærke baser.
* Nogle metaloxider: Metaloxider, der reagerer med vand for at danne hydroxider, betragtes også som baser. For eksempel reagerer calciumoxid (CaO) med vand og danner calciumhydroxid (Ca(OH)2).
* Ammoniak (NH3): Selvom det ikke er et metalhydroxid, er ammoniak en svag base, der reagerer med vand for at danne ammoniumioner (NH4+) og hydroxidioner (OH-).
Vigtig bemærkning: Styrken af en base afhænger af, hvor let den frigiver hydroxidioner i opløsning. Stærke baser dissocierer fuldstændigt til ioner i vand, mens svage baser kun delvist ioniserer.
Sidste artikelForståelse af carboxylsyrer:Virker R-COOH-forbindelser som syrer?
Næste artikelHydrogenatomer i molekyler:En hurtig guide
 Varme artikler
Varme artikler
-
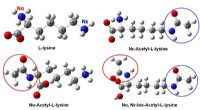 Raman og infrarød spektroskopi hjælper med at identificere forskellige acetylerede lysinerMolekylære strukturer af lysin og tre acetylerede lysiner. Kredit:Yao Guohua Et forskerhold ledet af prof. Huang Qing fra Hefei Institutes of Physical Science (HFIPS) under det kinesiske videnskabs
Raman og infrarød spektroskopi hjælper med at identificere forskellige acetylerede lysinerMolekylære strukturer af lysin og tre acetylerede lysiner. Kredit:Yao Guohua Et forskerhold ledet af prof. Huang Qing fra Hefei Institutes of Physical Science (HFIPS) under det kinesiske videnskabs -
 Undersøgelse af, hvordan tilføjelse af UV-behandling til vandklorering faktisk kan øge giftig tri…Kredit:He Zhao, Ching-Hua Huang, Chen Zhong, Penghui Du, Peizhe Sun Halobenzoquinoner (HBQer), som nye nye desinfektionsbiprodukter (DBPer), påvises ofte i drikkevand og svømmebassiner. Faktisk er
Undersøgelse af, hvordan tilføjelse af UV-behandling til vandklorering faktisk kan øge giftig tri…Kredit:He Zhao, Ching-Hua Huang, Chen Zhong, Penghui Du, Peizhe Sun Halobenzoquinoner (HBQer), som nye nye desinfektionsbiprodukter (DBPer), påvises ofte i drikkevand og svømmebassiner. Faktisk er -
 Beregning af varmeindekset:formel, betydning og praktisk brugAf Lee Johnson | Opdateret 30. august 2022 I videnskabelige sammenhænge er vi afhængige af objektive målinger, men dagligdags vejrudsigter bruger ofte varmeindekset at formidle, hvor varmt det faktis
Beregning af varmeindekset:formel, betydning og praktisk brugAf Lee Johnson | Opdateret 30. august 2022 I videnskabelige sammenhænge er vi afhængige af objektive målinger, men dagligdags vejrudsigter bruger ofte varmeindekset at formidle, hvor varmt det faktis -
 Væsentlige instrumenter til vejrudsigt:termometre, barometre, regnmålere og vindmålereHemera Technologies/AbleStock.com/Getty Images Jordens atmosfære er den eneste i vores solsystem, der understøtter et rigt billedtæppe af vejrbegivenheder. Nøjagtige prognoser er afgørende for hverda
Væsentlige instrumenter til vejrudsigt:termometre, barometre, regnmålere og vindmålereHemera Technologies/AbleStock.com/Getty Images Jordens atmosfære er den eneste i vores solsystem, der understøtter et rigt billedtæppe af vejrbegivenheder. Nøjagtige prognoser er afgørende for hverda
- Air India stopper med at bruge engangsplastik på fly
- Sag for axion-oprindelse af mørkt stof vinder trækkraft
- Spanien, Portugal kæmper med ekstrem tørke
- Når solen skinner direkte over kræftens tropiske i den nordlige halvkugle, hvad er Solstice det?
- Hvorfor er fluor mindre end ilt?
- Videnskabelige teorier er ikke blot formodninger - for at overleve skal de virke


