Forståelse af kemiske reaktioner:En omfattende vejledning
1. Opbrud af obligationer:
- Eksisterende kemiske bindinger mellem atomer i reaktantmolekylerne brydes. Dette kræver energi, som normalt leveres i form af varme.
2. Dannelse af nye obligationer:
- Atomer omarrangerer sig selv og danner nye bindinger for at skabe produktmolekyler. Denne proces frigiver ofte energi, nogle gange som varme eller lys.
3. Ændringer i kemisk sammensætning:
- Den kemiske sammensætning af de involverede stoffer ændres i takt med, at atomer omarrangeres, hvilket resulterer i, at der dannes nye stoffer.
4. Energiændringer:
- Kemiske reaktioner kan enten frigive energi (exotermisk) eller absorbere energi (endotermisk). Denne energiændring er vigtig for at forstå reaktionens spontanitet.
5. Bevarelse af messen:
- Den samlede masse af reaktanterne og den samlede masse af produkterne i en kemisk reaktion forbliver den samme. Dette er kendt som loven om bevarelse af masse.
Her er en analogi:
Forestil dig, at du har et Lego-sæt med klodser i forskellige farver. En kemisk reaktion ville være som at skille Lego-sættet ad og derefter bygge en helt ny struktur med de samme klodser, men arrangeret anderledes. Det samlede antal mursten forbliver det samme, men den endelige struktur er anderledes.
Faktorer, der påvirker kemiske reaktioner:
* Temperatur: Højere temperatur øger reaktionshastigheden.
* Koncentration: Højere koncentration af reaktanter fremskynder normalt reaktionen.
* Overfladeareal: Et større overfladeareal af reaktanter giver mulighed for flere kollisioner, hvilket fører til en hurtigere reaktion.
* Katalysator: En katalysator fremskynder reaktionen uden at blive forbrugt selv.
At forstå kemiske reaktioner er grundlæggende for mange områder, herunder kemi, biologi, medicin og teknik.
 Varme artikler
Varme artikler
-
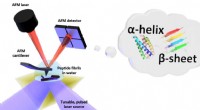 Formen i vand:Første nanoskalamålinger af biomolekylefoldning i væskeSkematisk af opsætningen for fototermisk induceret resonans (PTIR), som inkluderer en infrarød laserkilde og atomic force microscope (AFM) cantilever med en skarp spids, der rører prøven og vibrerer s
Formen i vand:Første nanoskalamålinger af biomolekylefoldning i væskeSkematisk af opsætningen for fototermisk induceret resonans (PTIR), som inkluderer en infrarød laserkilde og atomic force microscope (AFM) cantilever med en skarp spids, der rører prøven og vibrerer s -
 En udåndingstest for Parkinsons tidligt stadieKredit:American Chemical Society Symptomer på Parkinsons sygdom omfatter tremor, lugttab og neuropsykiatriske problemer. Imidlertid, mange mennesker bliver ikke diagnosticeret, før deres sygdom er
En udåndingstest for Parkinsons tidligt stadieKredit:American Chemical Society Symptomer på Parkinsons sygdom omfatter tremor, lugttab og neuropsykiatriske problemer. Imidlertid, mange mennesker bliver ikke diagnosticeret, før deres sygdom er -
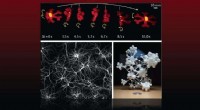 Forskere kortlægger fremskridt inden for arkitektonerede materialer, der reagerer på ydre stimuliI papir udgivet af Nature Reviews Materials , Lawrence Livermore National Laboratory-forskere giver et overblik over de fremskridt, der er gjort inden for responsive arkitektonerede materialer, der ka
Forskere kortlægger fremskridt inden for arkitektonerede materialer, der reagerer på ydre stimuliI papir udgivet af Nature Reviews Materials , Lawrence Livermore National Laboratory-forskere giver et overblik over de fremskridt, der er gjort inden for responsive arkitektonerede materialer, der ka -
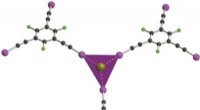 Koordinationskemi af anioner gennem halogenbindingsinteraktionerDetaljen af koordinationssfærerne af bromidanionen med Et3BuN+Br? Kredit:M. Fourmigué Mens en IUPAC-definition af hydrogenbinding først blev frigivet i 2011 efter årtiers diskussioner i det vide
Koordinationskemi af anioner gennem halogenbindingsinteraktionerDetaljen af koordinationssfærerne af bromidanionen med Et3BuN+Br? Kredit:M. Fourmigué Mens en IUPAC-definition af hydrogenbinding først blev frigivet i 2011 efter årtiers diskussioner i det vide


