Hydrogenbinding:Forståelse af kovalente bindinger i H₂-molekyler
Her er hvorfor:
* Deling af elektroner: Hvert brintatom har en elektron i sin yderste skal. For at opnå en stabil elektronkonfiguration (som helium) deler de begge deres elektroner. Dette skaber et delt elektronpar mellem de to brintatomer.
* Stærkt bånd: Det delte elektronpar skaber en stærk tiltrækning mellem de to positivt ladede brintkerner og den negativt ladede elektronsky. Det er det, der holder brintatomerne sammen til et molekyle.
* Lavere energi: Bindingsdannelsen frigiver energi, hvilket indikerer, at molekylet er i en lavere energitilstand end de to individuelle atomer.
Derfor er brintmolekylet et klassisk eksempel på en kovalent binding , hvor to atomer deler elektroner for at opnå stabilitet.
Sidste artikelMolær masse af ilt (O₂):Beregning og forklaring
Næste artikelTollens reagens:Forberedelse, sammensætning og reaktion forklaret
 Varme artikler
Varme artikler
-
 Sådan neutraliseres saltsyre sikkert med bagepulverAf Louis Gutierrez Opdateret 30. august 2022 eskaylim/iStock/GettyImages Bagepulver, eller natriumbicarbonat, er en mild base, der effektivt neutraliserer syrer, herunder den stærke saltsyre (HCl).
Sådan neutraliseres saltsyre sikkert med bagepulverAf Louis Gutierrez Opdateret 30. august 2022 eskaylim/iStock/GettyImages Bagepulver, eller natriumbicarbonat, er en mild base, der effektivt neutraliserer syrer, herunder den stærke saltsyre (HCl). -
 At snyde den nye coronavirus med et falsk håndtrykTransmissionselektronmikrografi af SARS-CoV-2-viruspartikler, isoleret fra en patient. Billede taget og farveforbedret på NIAID Integrated Research Facility (IRF) i Fort Detrick, Maryland. Kredit:NIAI
At snyde den nye coronavirus med et falsk håndtrykTransmissionselektronmikrografi af SARS-CoV-2-viruspartikler, isoleret fra en patient. Billede taget og farveforbedret på NIAID Integrated Research Facility (IRF) i Fort Detrick, Maryland. Kredit:NIAI -
 Elektriske vs. traditionelle bilbatterier:Vigtigste forskelle forklaretBLKstudio/Shutterstock På nutidens veje dominerer to adskilte køretøjskategorier:elektriske køretøjer (EVer) og konventionelle forbrændingsmotorer (ICE) biler. Selvom de deler et fælles mål – at tran
Elektriske vs. traditionelle bilbatterier:Vigtigste forskelle forklaretBLKstudio/Shutterstock På nutidens veje dominerer to adskilte køretøjskategorier:elektriske køretøjer (EVer) og konventionelle forbrændingsmotorer (ICE) biler. Selvom de deler et fælles mål – at tran -
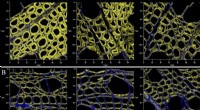 Kvantificering af ændringer i overfladekemi af træplanter under mikrobiel gæringORNL -forskere brugte sofistikerede laserscanningsteknikker til at sammenligne nedbrydningen af fermenteret populær (B) sammenlignet med ugæret populær (A), som de kvantificerede, for første gang, k
Kvantificering af ændringer i overfladekemi af træplanter under mikrobiel gæringORNL -forskere brugte sofistikerede laserscanningsteknikker til at sammenligne nedbrydningen af fermenteret populær (B) sammenlignet med ugæret populær (A), som de kvantificerede, for første gang, k


