Forstå Ammoniak's grundlæggende egenskaber:Hvorfor det er en base
* Det enlige par: Ammoniak har et ensomt elektronpar på nitrogenatomet. Dette enlige par er meget reaktivt og søger en positiv ladning at binde sig til.
* Protonacceptor: Når ammoniak støder på en proton (H⁺), accepterer det enlige par på nitrogenatomet let protonen og danner ammoniumionen (NH4⁺). Dette er den definerende karakteristik af en base - den accepterer protoner.
* Brønsted-Lowry Teori: Brønsted-Lowry-teorien om syrer og baser definerer en base som en protonacceptor. Ammoniak opfylder denne definition ved at reagere med syrer for at danne ammoniumionen.
* Ligevægt: Ammoniak's reaktion med vand er et godt eksempel på dets grundlæggende natur. I opløsning reagerer ammoniak med vand og danner ammoniumioner (NH4⁺) og hydroxidioner (OH⁻), hvilket øger hydroxidkoncentrationen og gør opløsningen alkalisk:
NH3(aq) + H2O(l) ⇌ NH4+(aq) + OH⁻(aq)
Opsummering: Ammoniak betragtes som en base, fordi den har et ensomt elektronpar, der let accepterer protoner, hvilket opfylder definitionen af en base ifølge Brønsted-Lowry-teorien. Dette er tydeligt i dets reaktion med vand, hvilket resulterer i en stigning i hydroxidionkoncentration og alkaliske egenskaber.
 Varme artikler
Varme artikler
-
 Forskere bestemmer aktiveringsmekanismen for G-proteinkoblede receptorerStruktur af den membranbundne β1-adrenerge receptor med vandeksponerede hulrum (blå), ikke tilgængelige for vand (gul) og tørre hulrum (magenta). Kredit:Biozentrum, Universitetet i Basel Næsten all
Forskere bestemmer aktiveringsmekanismen for G-proteinkoblede receptorerStruktur af den membranbundne β1-adrenerge receptor med vandeksponerede hulrum (blå), ikke tilgængelige for vand (gul) og tørre hulrum (magenta). Kredit:Biozentrum, Universitetet i Basel Næsten all -
 Hvor skadelige er nano-kobber og svampedræbende kombinationer i vandvejene?Feltprøveindsats, hvor intakte bentiske samfundskerner blev indsamlet. Kredit:Kay Ho En nyligt offentliggjort artikel i Miljøtoksikologi og kemi , Virkninger af mikroniseret og nano-kobberazol p
Hvor skadelige er nano-kobber og svampedræbende kombinationer i vandvejene?Feltprøveindsats, hvor intakte bentiske samfundskerner blev indsamlet. Kredit:Kay Ho En nyligt offentliggjort artikel i Miljøtoksikologi og kemi , Virkninger af mikroniseret og nano-kobberazol p -
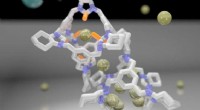 Burmolekyler fungerer som molekylsigter til adskillelse af brintisotopDannelse af en cocrystal forbedrer D2/H2-separationsydelsen. Kredit:University of Liverpool Et nyt hybridmateriale udviklet af forskere ved University of Liverpool kan bringe drømmen om kulstoffri
Burmolekyler fungerer som molekylsigter til adskillelse af brintisotopDannelse af en cocrystal forbedrer D2/H2-separationsydelsen. Kredit:University of Liverpool Et nyt hybridmateriale udviklet af forskere ved University of Liverpool kan bringe drømmen om kulstoffri -
 Karbonatstandarder sikrer bedre paleotermometreEn ny undersøgelse af Bernasconi et al. beskriver en samfundsindsats-InterCarb-for at standardisere den kemiske analyse kendt som carbonatklumpet-isotoptermometri, ved hjælp af fælles karbonatstandard
Karbonatstandarder sikrer bedre paleotermometreEn ny undersøgelse af Bernasconi et al. beskriver en samfundsindsats-InterCarb-for at standardisere den kemiske analyse kendt som carbonatklumpet-isotoptermometri, ved hjælp af fælles karbonatstandard
- Hvad gjorde Wilhelm Roentgen for videnskaben?
- Nyt værktøj til at forudsige polymeregenskaber
- Hvordan varierer bringthness fra størrelsen på Star?
- Rogue bølger ramte Hawaii fiskefartøj, der sank, siger ejer
- Tests viser, at højtemperatur superledende magneter er klar til fusion
- Beregningsmetoder til femte klasse Math


