Aluminiumchlorid (AlCl3):kovalent eller ionisk karakter?
* ionisk karakter: Aluminium (Al) er et metal, og klor (Cl) er et ikke-metal. Metaller har en tendens til at tabe elektroner og danne positive ioner (kationer), mens ikke-metaller har tendens til at få elektroner og danne negative ioner (anioner). Denne forskel i elektronegativitet fører til en ionisk interaktion.
* Kovalent karakter: Elektronegativitetsforskellen mellem aluminium og klor er ikke ekstremt stor. Dette fører til en betydelig grad af kovalent karakter i bindingerne. Elektronerne overføres ikke fuldt ud fra aluminium til klor, men deles snarere til en vis grad.
Opsummering:
* AlCl3 udviser karakteristika for både ionisk og kovalent binding.
* Bindingen i AlCl3 beskrives bedst som polær kovalent .
* Det er vigtigt at bemærke, at bindingen i de fleste forbindelser falder et sted på et spektrum mellem rent ionisk og rent kovalent.
 Varme artikler
Varme artikler
-
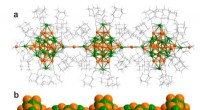 Teknik til fremstilling af funktionelle materialer baseret på polymerer af metalklyngerFigur a:Visualisering af en lineær polymer af 34-atom sølv-guldklyngerne med metal-metalbinding mellem klyngerne i vandret retning (guld:orange, sølv:grøn, ligandmolekyler (ethynyladamantan) er vist m
Teknik til fremstilling af funktionelle materialer baseret på polymerer af metalklyngerFigur a:Visualisering af en lineær polymer af 34-atom sølv-guldklyngerne med metal-metalbinding mellem klyngerne i vandret retning (guld:orange, sølv:grøn, ligandmolekyler (ethynyladamantan) er vist m -
 En strømlinet tilgang til bestemmelse af termiske egenskaber for krystallinske faste stoffer og leg…Et neuralt netværk, der bærer fuld krystal -symmetri, muliggør effektiv træning af krystallinske faste stoffer. Kredit:Massachusetts Institute of Technology I et essay i september 2020 i Naturene
En strømlinet tilgang til bestemmelse af termiske egenskaber for krystallinske faste stoffer og leg…Et neuralt netværk, der bærer fuld krystal -symmetri, muliggør effektiv træning af krystallinske faste stoffer. Kredit:Massachusetts Institute of Technology I et essay i september 2020 i Naturene -
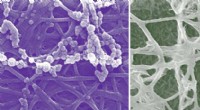 Ny cellulær indsigt i knogleudviklingCalciumphosphatmineralisering forekommer i både ekstra- og intrafibrillære rum af kollagen (venstre og højre billeder, henholdsvis). Ingeniører ved Washington University i St. Louis forsøgte eksperime
Ny cellulær indsigt i knogleudviklingCalciumphosphatmineralisering forekommer i både ekstra- og intrafibrillære rum af kollagen (venstre og højre billeder, henholdsvis). Ingeniører ved Washington University i St. Louis forsøgte eksperime -
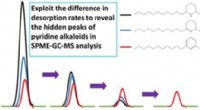 Nyligt identificerede forbindelser kan hjælpe med at give ildmyrer deres brodKredit:American Chemical Society hjemmehørende i Sydamerika, importerede ildmyrer har nu spredt sig til dele af Nordamerika og andre steder i verden. Disse invasive skadedyr har smertefulde stik,
Nyligt identificerede forbindelser kan hjælpe med at give ildmyrer deres brodKredit:American Chemical Society hjemmehørende i Sydamerika, importerede ildmyrer har nu spredt sig til dele af Nordamerika og andre steder i verden. Disse invasive skadedyr har smertefulde stik,
- Hvordan opbevares energikilden, når den er kommet sig i olie?
- Forskere foretager en omfattende gennemgang af forberedelse af MOF-baserede flammehæmmere via koord…
- Jorden vs. Mars:En sammenlignende undersøgelse af ligheder og forskelle
- Shark
- Er en smeltende smør fysisk forandring eller kemisk forandring?
- Vil et målebånd på 300 cm nå langs brættet, der er 2,75 m lang, forklare Wit -beregning?


