At forstå atomare egenskaber:Beyond Valence Electron Size
Her er hvorfor:
* Antal valenselektroner: Antallet af valenselektroner er en vigtig faktor i bestemmelsen af et atoms kemiske reaktivitet, bindingsadfærd og evne til at danne ioner.
* Effektiv nuklear ladning: Den effektive kerneladning (den positive nettoladning, som valenselektroner oplever) påvirker størrelsen af atomet og tiltrækningen mellem kernen og valenselektronerne. En højere effektiv nuklear ladning resulterer i et mindre atom.
* Elektronkonfiguration: Ordningen af elektroner i forskellige energiniveauer og underniveauer påvirker et atoms egenskaber. For eksempel påvirker tilstedeværelsen af d-orbitaler i overgangsmetaller deres reaktivitet og bindingsegenskaber.
* Afskærmningseffekt: Indre elektroner beskytter valenselektroner fra kernens fulde tiltrækning, hvilket påvirker størrelsen og energien af valenselektronerne.
Opsummering:
Mens størrelsen af valenselektroner er en faktor, bidrager andre aspekter, såsom antallet af valenselektroner, effektiv nuklear ladning, elektronkonfiguration og afskærmningseffekt, alle væsentligt til at bestemme et atoms egenskaber.
Sidste artikelAluminiumchlorid (AlCl3):kovalent eller ionisk karakter?
Næste artikelOzon (O3):Forståelse af molekylær polaritet og binding
 Varme artikler
Varme artikler
-
 Uforgængelig virus giver hemmelighed ved at skabe utroligt holdbare materialerPeter M. Kasson, M.D., Ph.d., (til venstre) og Edward H. Egelman, Ph.d., har låst op for hemmelighederne ved en næsten uforgængelig virus, muligvis tillader forskere at udnytte sine bemærkelsesværdige
Uforgængelig virus giver hemmelighed ved at skabe utroligt holdbare materialerPeter M. Kasson, M.D., Ph.d., (til venstre) og Edward H. Egelman, Ph.d., har låst op for hemmelighederne ved en næsten uforgængelig virus, muligvis tillader forskere at udnytte sine bemærkelsesværdige -
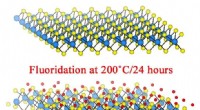 Fluor strømmer ind, laver materiale metalFluorerende todimensionelt wolframdisulfid tilføjer metalliske øer til den syntetiske halvleder, sammen med unikke optiske og magnetiske egenskaber, ifølge forskere ved Rice University. Kredit:Ajayan
Fluor strømmer ind, laver materiale metalFluorerende todimensionelt wolframdisulfid tilføjer metalliske øer til den syntetiske halvleder, sammen med unikke optiske og magnetiske egenskaber, ifølge forskere ved Rice University. Kredit:Ajayan -
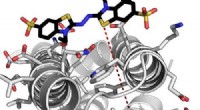 Kunstige enzymfunktioner samt naturlig versionBeregningsmodel for et yderst effektivt de novo -enzym, der interagerer med et af dets substrater. Den røde stiplede linje angiver elektrontunnelafstanden mellem det proteinbundne hæmmolekyle og det b
Kunstige enzymfunktioner samt naturlig versionBeregningsmodel for et yderst effektivt de novo -enzym, der interagerer med et af dets substrater. Den røde stiplede linje angiver elektrontunnelafstanden mellem det proteinbundne hæmmolekyle og det b -
 Biologisk inspireret membran renser kulfyret røg for drivhusgasserSandia National Laboratories-stipendiat og University of New Mexico-regentprofessor Jeff Brinker ledede arbejdet med at udvikle det billige memzyme, der er i stand til at fjerne kulrøg for kuldioxid,
Biologisk inspireret membran renser kulfyret røg for drivhusgasserSandia National Laboratories-stipendiat og University of New Mexico-regentprofessor Jeff Brinker ledede arbejdet med at udvikle det billige memzyme, der er i stand til at fjerne kulrøg for kuldioxid,
- Hvordan påvirker forvitring landet?
- Solsystemer kan bruges som ressourcer til planteproduktivitet, undersøgelse viser
- Forskning afslører hemmeligheder om jernopbevaring i alger
- Sand eller falsk svampet mesofyl er celler i et blad?
- Hvad vil Light Wave gøre, når de bevæger sig fra tomt rum til stof, der består af forskellige ga…
- Sådan opbygger du støtte til ambitiøse klimaindsatser i 4 trin


