Ozon (O3):Forståelse af molekylær polaritet og binding
* Molekylær geometri: Ozon har en bøjet molekylær geometri. Dette betyder, at de tre oxygenatomer ikke er arrangeret i en lige linje, hvilket forårsager en ujævn fordeling af elektrontætheden.
* Polar obligationer: Hver oxygen-iltbinding i ozon er en polær kovalent binding. Dette skyldes, at oxygen er mere elektronegativt end de andre oxygenatomer, hvilket trækker de delte elektroner tættere på sig selv.
* Symmetri: På trods af de polære bindinger er molekylet symmetrisk. De individuelle bindingsdipoler udligner hinanden, hvilket resulterer i et nul netto dipolmoment .
Derfor, selvom ozon har polære bindinger, gør dens symmetriske form det til et ikke-polært molekyle.
 Varme artikler
Varme artikler
-
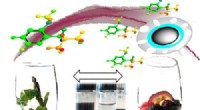 Magnetisk behandling kan hjælpe med at fjerne bismag fra vineKredit:American Chemical Society Magnetiske nanopartikler knyttet til polymerer er med succes blevet brugt til at målrette og fjerne uønskede smagsstoffer fra vin. Forskere ved University of Adel
Magnetisk behandling kan hjælpe med at fjerne bismag fra vineKredit:American Chemical Society Magnetiske nanopartikler knyttet til polymerer er med succes blevet brugt til at målrette og fjerne uønskede smagsstoffer fra vin. Forskere ved University of Adel -
 Hård kærlighed:Intens genskin hjælper næste generations solteknologi gennem den akavede fase660 nm) er fra fase-separeret perovskit drevet af lav-intensitet konfokal mikroskop scanning laser. Kredit:ARC Center of Excellence in Exciton Science Forskere i Australien har løst en grundlæggen
Hård kærlighed:Intens genskin hjælper næste generations solteknologi gennem den akavede fase660 nm) er fra fase-separeret perovskit drevet af lav-intensitet konfokal mikroskop scanning laser. Kredit:ARC Center of Excellence in Exciton Science Forskere i Australien har løst en grundlæggen -
 Kemisk tiltrækning giver klapperslange peptid bid på superbugsKredit:University of Queensland Forskere har vist, hvorfor et fragment af et protein fra klappekirtlen hos klapperslanger kunne være grundlaget for et alternativ til konventionelle antibiotika. U
Kemisk tiltrækning giver klapperslange peptid bid på superbugsKredit:University of Queensland Forskere har vist, hvorfor et fragment af et protein fra klappekirtlen hos klapperslanger kunne være grundlaget for et alternativ til konventionelle antibiotika. U -
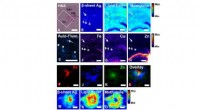 Kombineret billeddannelsestilgang karakteriserer plaques forbundet med Alzheimers sygdomHistologi, FTIR, XFM, og vævsautofluorescensbilleddannelse af Aβ-plaques. Kredit:University of Adelaide Australske synkrotron røntgen og infrarød billeddannelsesteknikker er blevet brugt i en kraf
Kombineret billeddannelsestilgang karakteriserer plaques forbundet med Alzheimers sygdomHistologi, FTIR, XFM, og vævsautofluorescensbilleddannelse af Aβ-plaques. Kredit:University of Adelaide Australske synkrotron røntgen og infrarød billeddannelsesteknikker er blevet brugt i en kraf
- Hvad spiser spiser?
- Forstærker anden harmonisk generation med TMD's monolag
- Forskere sammenligner den globale temperaturvariabilitet i glaciale og mellemistider
- Hvad er indtrængning af havvand? En hydrogeolog forklarer den skiftende balance mellem fersk- og sa…
- <p> Som et naturligt forekommende organisk opløsningsmiddel, der ofte bruges til fremstilling af pl…
- Hvad er forskellige gasser, der påvirker den globale opvarmning?


