Beregn damptryk for HgCl₂-vandopløsning:Raoults lov forklaret
Forstå begreberne
* Damptryk: Det tryk, der udøves af dampen fra en væske i ligevægt med dens væskefase.
* Raoults lov: Angiver, at partialdamptrykket af et opløsningsmiddel i en opløsning er lig med damptrykket af det rene opløsningsmiddel ganget med dets molfraktion i opløsningen.
* Molbrøk: Forholdet mellem mol af en komponent og det samlede antal mol i en opløsning.
Trin
1. Identificer opløsningsmidlet og det opløste stof:
* Opløsningsmiddel:Vand (H₂O)
* Opløst stof:kviksølv(II)chlorid (HgCl₂)
2. Bestem damptrykket for rent vand:
* Ved 25°C er damptrykket af rent vand cirka 23,76 torr (du kan finde denne værdi i en tabel eller online).
3. Beregn molfraktionen af vand:
* Da molfraktionen af HgCl2 er 0,163, er molfraktionen af vand (H2O):
* Molfraktion af H2O =1 - molfraktion af HgCl2 =1 - 0,163 =0,837
4. Anvend Raoults lov:
* Opløsningens damptryk =(molfraktion af H₂O) * (Damptryk af ren H₂O)
* Opløsningens damptryk =(0,837) * (23,76 torr)
* Opløsningens damptryk ≈ 19,88 torr
Damptrykket af vandopløsningen indeholdende 0,163 molfraktion HgCl2 ved 25°C er derfor ca. 19,88 torr.
Vigtig bemærkning:
* Denne beregning antager, at HgCl₂ er et ikke-flygtigt opløst stof, hvilket betyder, at det ikke bidrager væsentligt til opløsningens damptryk.
* Det faktiske damptryk af opløsningen kan være lidt anderledes på grund af mulige vekselvirkninger mellem opløsningsmidlet og det opløste stofs molekyler.
Sidste artikelBlyfri benzinproduktion:En trin-for-trin guide
Næste artikelSølvnitrat og saltsyrereaktion:kemi forklaret
 Varme artikler
Varme artikler
-
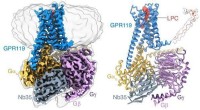 Undersøgelse afslører ligandgenkendelsesmekanisme for forældreløs receptor GPR119Identifikation af LPCet bundet til GPR119-Gs-komplekset ved hjælp af cryo-EM. Kredit:Peiyu Xu fra H. Eric Xus laboratorium Metaboliske sygdomme, herunder diabetes, fedtlever og fedme, er blevet en
Undersøgelse afslører ligandgenkendelsesmekanisme for forældreløs receptor GPR119Identifikation af LPCet bundet til GPR119-Gs-komplekset ved hjælp af cryo-EM. Kredit:Peiyu Xu fra H. Eric Xus laboratorium Metaboliske sygdomme, herunder diabetes, fedtlever og fedme, er blevet en -
 Ny indsigt i rotavirusmekanik kan føre til forbedrede behandlingerKunstnerisk gengivelse af rotaviruspartikeldissektionsprocessen, udført med atomkraftmikroskopi. Kredit:Billede skabt af Scixel (scixel.es/), under instruktionerne af D. Luque og P. J. de Pablo. F
Ny indsigt i rotavirusmekanik kan føre til forbedrede behandlingerKunstnerisk gengivelse af rotaviruspartikeldissektionsprocessen, udført med atomkraftmikroskopi. Kredit:Billede skabt af Scixel (scixel.es/), under instruktionerne af D. Luque og P. J. de Pablo. F -
 Fælder for energikildemolekyler i cellerKredit:Natalia Deryugina Et team af forskere, inklusive en RUDN-kemiker, har syntetiseret nye molekyler, der tilhører klassen af calixarener, skållignende hule strukturer. Disse stoffer ser ud t
Fælder for energikildemolekyler i cellerKredit:Natalia Deryugina Et team af forskere, inklusive en RUDN-kemiker, har syntetiseret nye molekyler, der tilhører klassen af calixarener, skållignende hule strukturer. Disse stoffer ser ud t -
 Hvordan varme driver kemiske reaktioner:fra energi til ligevægtSom en form for energi påvirker varme næsten alle kemiske processer. Det kan igangsætte reaktioner, opretholde dem og diktere deres hastighed og retning. Varme i kemiske reaktioner Reaktioner kræver
Hvordan varme driver kemiske reaktioner:fra energi til ligevægtSom en form for energi påvirker varme næsten alle kemiske processer. Det kan igangsætte reaktioner, opretholde dem og diktere deres hastighed og retning. Varme i kemiske reaktioner Reaktioner kræver
- Hvor akustik er relateret til fysik?
- Tværkurrikulære geometriaktiviteter til fly og faste former
- Hvilken energi konverteres, når du skubber en magnetbevægelse gennem ledningen?
- I Sibirien, Kinesisk efterspørgsel efter forhistoriske stødtænder giver næring til mammutsus
- Forskere viser, hvordan dødelige vulkanske fænomener bevæger sig
- Dette er organismer, der kommer fra den samme celle og genetisk identiske med hinanden?


