Sølvnitrat og saltsyrereaktion:kemi forklaret
Her er den afbalancerede kemiske ligning:
AgNO3 (aq) + HCl (aq) → AgCl (s) + HNO3 (aq)
Her er en oversigt over reaktionen:
* Sølvnitrat (AgNO₃) er en opløselig ionforbindelse, der dissocierer i vand til sølvioner (Ag⁺) og nitrationer (NO3⁻).
* Saltsyre (HCl) er en stærk syre, der dissocierer i vand til hydrogenioner (H⁺) og chloridioner (Cl⁻).
* Sølvchlorid (AgCl) er en uopløselig ionforbindelse, hvilket betyder, at den ikke let opløses i vand. Når Ag⁺-ioner fra sølvnitrat og Cl⁻-ioner fra saltsyre samles, danner de et fast bundfald, der falder ud af opløsningen.
* Salpetersyre (HNO₃) forbliver opløst i opløsningen som en opløselig ionforbindelse.
Denne reaktion bruges i forskellige applikationer, herunder:
* Test for chloridioner: Dannelsen af et hvidt bundfald er en klassisk test for tilstedeværelsen af chloridioner i en opløsning.
* Sølvhalogenfotografering: Sølvchlorid, bromid og iodid bruges i fotografisk film til at fange lys.
* Syntese af andre sølvforbindelser: Denne reaktion kan bruges som udgangspunkt for syntesen af andre sølvforbindelser.
Bemærk: Reaktionen er meget eksoterm, hvilket betyder, at den frigiver varme. Derfor er det vigtigt at håndtere reaktionen med forsigtighed og passende sikkerhedsforanstaltninger.
Sidste artikelBeregn damptryk for HgCl₂-vandopløsning:Raoults lov forklaret
Næste artikelSaltvandspoolkemikalier:En omfattende guide
 Varme artikler
Varme artikler
-
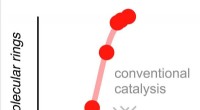 Kemi:Adgang til forbudte ringeAutokatalytisk dannelse af molekylære ringe med de nye uortodokse anion-π katalysatorer (rød) sammenlignet med konventionel adfærd (grå). Kredit:University of Geneva Cykliske molekyler er overalt,
Kemi:Adgang til forbudte ringeAutokatalytisk dannelse af molekylære ringe med de nye uortodokse anion-π katalysatorer (rød) sammenlignet med konventionel adfærd (grå). Kredit:University of Geneva Cykliske molekyler er overalt, -
 En strandelskers drøm:Et skridt mod langtidsholdbar solcremeKredit:Marina Shemesh/offentligt domæne I en perfekt verden, folk ville flittigt genanvende solskærmen hvert par timer for at beskytte deres sarte hud mod skadelig solstråling. Men i virkeligheden
En strandelskers drøm:Et skridt mod langtidsholdbar solcremeKredit:Marina Shemesh/offentligt domæne I en perfekt verden, folk ville flittigt genanvende solskærmen hvert par timer for at beskytte deres sarte hud mod skadelig solstråling. Men i virkeligheden -
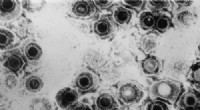 Kryo-elektronmikroskopi afslører almindelig herpesvirusstrukturHerpes simplex virus. Kredit:CDC For første gang, forskere har været i stand til at bruge kryo-elektronmikroskopi, at afsløre den detaljerede struktur af den almindelige herpesvirus. Forskere ved
Kryo-elektronmikroskopi afslører almindelig herpesvirusstrukturHerpes simplex virus. Kredit:CDC For første gang, forskere har været i stand til at bruge kryo-elektronmikroskopi, at afsløre den detaljerede struktur af den almindelige herpesvirus. Forskere ved -
 En ny metode til installation af svovl i komplekse molekylerForskere, der arbejder i laboratoriet i Ben Shen, Ph.d., hos Scripps Research, Florida har fundet en ny familie af svovlinstallerende enzymer ved at udvinde bakteriernes genomer i deres samling af mik
En ny metode til installation af svovl i komplekse molekylerForskere, der arbejder i laboratoriet i Ben Shen, Ph.d., hos Scripps Research, Florida har fundet en ny familie af svovlinstallerende enzymer ved at udvinde bakteriernes genomer i deres samling af mik
- GPM observerer den tropiske cyklon Eliakim dannes nær Madagaskar
- Økonomiske forstyrrelser og forstyrrelser i fødevareforsyningskæden bringer den globale fødevare…
- Drone-baseret tidlig detektionssystem til at overvåge ændringer i Amazonas
- Hvad er antallet af kromosomer i zygoten, hvis kønsceller eller kønsceller indeholder 12 hver?
- De miljømæssige omkostninger ved cryptocurrency-miner
- Hvordan Volvox fik sin rille


