Forståelse af syrer:egenskaber, karakteristika og definitioner
Almindelige karakteristika for syrer:
* Smag: Syrer smager typisk surt. (Vær forsigtig, smag aldrig kemikalier!)
* Reaktion med baser: Syrer reagerer med baser og danner salte og vand. Dette er kendt som neutralisering.
* Reaktion med metaller: Mange syrer reagerer med metaller for at producere brintgas.
* Effekt på indikatorer: Syrer ændrer farven på visse indikatorer, som lakmuspapir (gør det rødt).
* pH: Syrer har en pH-værdi på under 7.
Definitioner af syrer:
1. Arrhenius Definition: Dette er den enkleste og mest kendte definition. Den siger, at en syre er et stof, der producerer hydrogenioner (H+), når det opløses i vand.
* Eksempel:HCl (saltsyre) dissocierer i vand og danner H+ og Cl-ioner.
2. Brønsted-Lowry Definition: Denne bredere definition siger, at en syre er et stof, der kan donere en proton (H+) til et andet stof.
* Eksempel:I reaktionen mellem HCl og vand donerer HCl en proton til vand og danner H3O+ (hydroniumion) og Cl-.
3. Lewis Definition: Dette er den mest generelle definition. Den siger, at en syre er et stof, der kan acceptere et par elektroner.
* Eksempel:Bortrifluorid (BF3) kan acceptere et par elektroner fra ammoniak (NH3).
Nøglepunkter at huske:
* Arrhenius-definitionen er et specialtilfælde af Brønsted-Lowry-definitionen.
* Lewis-definitionen er den mest generelle og omfatter både Brønsted-Lowry- og Arrhenius-syrer.
* Syrernes egenskaber er direkte relateret til tilstedeværelsen af hydrogenioner (H+).
Lad mig vide, hvis du har andre spørgsmål om syrer!
Sidste artikelBeregning af svovlmol i svovlsyre (H₂SO₄)
Næste artikelKlortilstande af stof:gas, væske og fast stof forklaret
 Varme artikler
Varme artikler
-
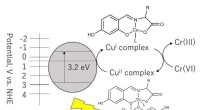 Reduktion ved reduktion:Ny tilgang til at afbøde chromforurening i spildevandChromforurening i spildevand kan afbødes ved at omdanne Cr(VI) til Cr(III) gennem en fotokemisk reaktion, der involverer kobberkomplekser. Kredit:Takashiro Akitsu, Tokyos Videnskabsuniversitet Gru
Reduktion ved reduktion:Ny tilgang til at afbøde chromforurening i spildevandChromforurening i spildevand kan afbødes ved at omdanne Cr(VI) til Cr(III) gennem en fotokemisk reaktion, der involverer kobberkomplekser. Kredit:Takashiro Akitsu, Tokyos Videnskabsuniversitet Gru -
 Computervision hjælper forskere med at studere lithium-ion-batterierEn ny computervisionsalgoritme til at identificere partikler i en lithium-ion batteri katode har hjulpet forskere med at spore katodens nedbrydning over tid. Kredit:Yijin Liu/SLAC National Accelerator
Computervision hjælper forskere med at studere lithium-ion-batterierEn ny computervisionsalgoritme til at identificere partikler i en lithium-ion batteri katode har hjulpet forskere med at spore katodens nedbrydning over tid. Kredit:Yijin Liu/SLAC National Accelerator -
 Video:Hvordan blyanter kan hjælpe os med at forstå fremtiden for alting (Alex vil have en jetpack)Kredit:The American Chemical Society Kemiverdenen har været begejstret for muligheden for buckyballs, grafen og kulstofnanorør i årtier. Men videnskaben har taget lang tid at indhente hypen. Så
Video:Hvordan blyanter kan hjælpe os med at forstå fremtiden for alting (Alex vil have en jetpack)Kredit:The American Chemical Society Kemiverdenen har været begejstret for muligheden for buckyballs, grafen og kulstofnanorør i årtier. Men videnskaben har taget lang tid at indhente hypen. Så -
 Konstrueret mikrobiel produktion af druesmagBillede 1: Konstruerede bakterier, der producerer druesmag. Kredit:Korea Advanced Institute of Science and Technology (KAIST) Forskere rapporterer om en mikrobiel metode til fremstilling af en ku
Konstrueret mikrobiel produktion af druesmagBillede 1: Konstruerede bakterier, der producerer druesmag. Kredit:Korea Advanced Institute of Science and Technology (KAIST) Forskere rapporterer om en mikrobiel metode til fremstilling af en ku
- Hvor mange iltatomer er til stede i en 14,0 g prøve af Cu (NO3) 2?
- Dette er de grundlæggende byggesten af proteiner?
- Hvorfor er celler i mange-cellede organismer forskellige?
- Hvordan dannes jord?
- Hvad sker der med plante- og dyerceller, når de placeres i hypertoniske, hypotoniske og isotoniske …
- Er det sandt, eller falseøiske arter er en gruppe af lignende organismer, der kan parre sig med hin…


