Bevarelse af massetal i kemiske ligninger:En omfattende vejledning
Reaktanternes samlede masseantal er lig med produkternes samlede masseantal.
Sådan fungerer det:
* Massenummer: Et atoms massetal er summen af dets protoner og neutroner.
* Kemiske reaktioner: I kemiske reaktioner bliver atomer omarrangeret, ikke skabt eller ødelagt. Antallet af protoner og neutroner i hvert atom forbliver det samme.
* Bevarelse: Det betyder, at det samlede antal protoner og neutroner på reaktantsiden af ligningen skal være lig med det samlede antal på produktsiden.
Eksempel:
Overvej forbrænding af metan (CH₄):
CH4 + 2O2 → CO2 + 2H2O
* Reaktanter:
* CH4:Massetal =12 (C) + 4 (H) =16
* 2O2:Massetal =2 * 32 (O) =64
* Total reaktantmasseantal =16 + 64 =80
* Produkter:
* CO₂:Massetal =12 (C) + 2 * 16 (O) =44
* 2H2O:Massetal =2 * (2 (H) + 16 (O)) =36
* Samlet produktmasseantal =44 + 36 =80
Det totale massetal på reaktantsiden (80) er lig med det samlede massetal på produktsiden (80). Derfor er princippet om bevarelse af massetal opfyldt i denne kemiske ligning.
Nøglepunkter:
* Princippet om bevarelse af massetal er også kendt som bevarelse af nukleoner .
* Det er vigtigt at huske, at dette princip gælder for nukleare reaktioner også, hvor antallet af protoner og neutroner kan ændre sig.
* Afbalancering af kemiske ligninger sikrer bevarelsen af massetal.
Sig til, hvis du har yderligere spørgsmål!
Sidste artikelForståelse af partikler:sammensætning og kemisk beskaffenhed
Næste artikelKaliumoxidationstal:Forståelse af +1 og undtagelser
 Varme artikler
Varme artikler
-
 Brug af elementer i anlæg til at øge brændselscelleeffektiviteten og samtidig reducere omkostning…Qiliang Wei arbejder på en canadisk lyskildestrålelinje. Kredit:Canadian Light Source Forskere fra Institut National de la Recherche Scientifique, Québec kigger ind i siv, høje vådområder planter,
Brug af elementer i anlæg til at øge brændselscelleeffektiviteten og samtidig reducere omkostning…Qiliang Wei arbejder på en canadisk lyskildestrålelinje. Kredit:Canadian Light Source Forskere fra Institut National de la Recherche Scientifique, Québec kigger ind i siv, høje vådområder planter, -
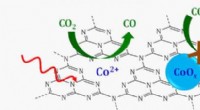 Lysaktiveret, single-ion katalysator nedbryder kuldioxidSkematisk over en enkeltstedskatalysator, hvor enkelte koboltioner (CO 2 +) understøttet på et grafitisk kulstofnitrogenlag (C3N4) reducerer kuldioxid (CO 2 ) til carbonmonoxid (CO) i nærvær af sy
Lysaktiveret, single-ion katalysator nedbryder kuldioxidSkematisk over en enkeltstedskatalysator, hvor enkelte koboltioner (CO 2 +) understøttet på et grafitisk kulstofnitrogenlag (C3N4) reducerer kuldioxid (CO 2 ) til carbonmonoxid (CO) i nærvær af sy -
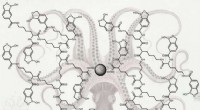 Kemisk blæksprutte fanger luskede kræftspor, spor glykoproteinerDelene, der er formet som en hexagon-pentagon combo, er benzoboroxoler, som gør store glykoproteinfangere, og de er syet sammen for at danne meget fleksible arme med lang rækkevidde. I midten er en ma
Kemisk blæksprutte fanger luskede kræftspor, spor glykoproteinerDelene, der er formet som en hexagon-pentagon combo, er benzoboroxoler, som gør store glykoproteinfangere, og de er syet sammen for at danne meget fleksible arme med lang rækkevidde. I midten er en ma -
 Opdagelse af nye lægemidler er en lang og dyr proces:Kemiske forbindelser, som duper screeningsvær…Kredit:Pixabay/CC0 Public Domain Moderne lægemiddelopdagelse er en dyr og kompliceret proces. Hundredvis af videnskabsmænd og mindst et årti er ofte påkrævet for at producere en enkelt medicin. Et
Opdagelse af nye lægemidler er en lang og dyr proces:Kemiske forbindelser, som duper screeningsvær…Kredit:Pixabay/CC0 Public Domain Moderne lægemiddelopdagelse er en dyr og kompliceret proces. Hundredvis af videnskabsmænd og mindst et årti er ofte påkrævet for at producere en enkelt medicin. Et


