Hvorfor kovalente forbindelser er dårlige elektriske ledere:en forklaring
* Ingen gratis gebyrer: I kovalente forbindelser deles elektroner mellem atomer for at danne stærke kovalente bindinger. Disse elektroner er tæt bundet og er ikke frie til at bevæge sig uafhængigt. Der er ingen frie ioner eller elektroner til at bære en elektrisk strøm.
* Neutrale molekyler: Kovalente forbindelser danner typisk neutrale molekyler. Da der ikke er nogen adskillelse af ladning i molekylet, er der ingen ladede partikler til at transportere elektricitet.
* Svage intermolekylære kræfter: Kræfterne mellem kovalente molekyler (som van der Waals-kræfter eller hydrogenbindinger) er meget svagere end de ioniske bindinger, der findes i ioniske forbindelser. Dette betyder, at molekylerne er mindre tilbøjelige til at bryde fra hinanden til ioner, der kan lede elektricitet.
I modsætning hertil leder ioniske opløsninger elektricitet godt, fordi:
* Gratis ioner: Ioniske forbindelser dissocierer i opløsning og frigiver frie ioner, der kan bevæge sig og bære en elektrisk strøm.
* Ladede partikler: Tilstedeværelsen af ladede ioner muliggør strømmen af elektricitet.
Eksempel:
* Sukker (kovalent) i vand: Sukker opløses i vand, men molekylerne forbliver intakte. Løsningen leder ikke elektricitet.
* Salt (ionisk) i vand: Salt opløses i vand og opløses i Na+ og Cl-ioner. Løsningen leder elektricitet.
Opsummering: Kovalente opløsninger har dårlig elektrisk ledningsevne, fordi de mangler frie ladninger (ioner eller elektroner) til at bære en elektrisk strøm.
 Varme artikler
Varme artikler
-
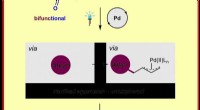 Undervisning i gamle overgangsmetaller nye tricks:Kemikere aktiverer palladiumkatalyse ved lysKemisk illustration af den nye metode til fremstilling af π-allylpalladiumkomplekser ved radikal kemi Kredit:Frank Glorius Ved fremstilling af forbindelser, kemikere har det grundlæggende mål at f
Undervisning i gamle overgangsmetaller nye tricks:Kemikere aktiverer palladiumkatalyse ved lysKemisk illustration af den nye metode til fremstilling af π-allylpalladiumkomplekser ved radikal kemi Kredit:Frank Glorius Ved fremstilling af forbindelser, kemikere har det grundlæggende mål at f -
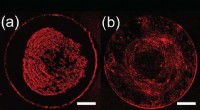 Ny fremstillingsteknik kan forbedre det almindelige problem inden for printteknologiFor figur A, der er partikeltransport til spidsen af måldråben, og der dannes en tæt midteraflejring. For figur B, den endelige kortlagte indbetaling er mere ensartet. Kredit: Langmuir En ny fr
Ny fremstillingsteknik kan forbedre det almindelige problem inden for printteknologiFor figur A, der er partikeltransport til spidsen af måldråben, og der dannes en tæt midteraflejring. For figur B, den endelige kortlagte indbetaling er mere ensartet. Kredit: Langmuir En ny fr -
 Optiske overtoner til solcellerAnalogt med et fænomen kendt for musikinstrumenter, når overtoner af to forskellige grundtoner kommer i resonans, forskere fra LMU München har fundet en ny effekt med hensyn til optisk excitation af l
Optiske overtoner til solcellerAnalogt med et fænomen kendt for musikinstrumenter, når overtoner af to forskellige grundtoner kommer i resonans, forskere fra LMU München har fundet en ny effekt med hensyn til optisk excitation af l -
 Ny sensorteknologi muliggør superfølsom live overvågning af menneskelige biomolekylerEt stillbillede fra videoen, der forklarer konceptet. Kredit:ICMS Animation Studio Menneskekroppen er en ekstremt kompleks molekylær maskine, hvis detaljer kan følges gennem visse stoffer; såkaldt
Ny sensorteknologi muliggør superfølsom live overvågning af menneskelige biomolekylerEt stillbillede fra videoen, der forklarer konceptet. Kredit:ICMS Animation Studio Menneskekroppen er en ekstremt kompleks molekylær maskine, hvis detaljer kan følges gennem visse stoffer; såkaldt
- Hvad er udviklingskontroversen?
- Hvad sker der, når du blander calciumhydroxid og ammoniumchlorid?
- Algoritme forudsiger sammensætninger af nye materialer
- Uformelle og illegale boliger er i fremmarch, da vores byer ikke kan tilbyde billige steder at bo
- En ny undersøgelse viser, hvordan solen permanent kunne fange slyngelplaneter
- Troen på læringsstile kan være skadelig


