Ædelgasser vs. halogener:Forståelse af første ioniseringsenergiforskelle
1. Fuld Valence Shell: Ædelgasser har en komplet oktet (eller duet for helium) i deres valensskal. Det betyder, at deres yderste elektroner holdes tæt fast af kernen, hvilket resulterer i en meget stabil elektronisk konfiguration. Fjernelse af en elektron fra denne stabile konfiguration kræver en betydelig mængde energi, derfor den høje ioniseringsenergi.
2. Mindre atomstørrelse: Ædelgasser er mindre i størrelse end halogener. Denne mindre størrelse betyder, at de yderste elektroner er tættere på kernen og oplever en stærkere elektrostatisk tiltrækning. Fjernelse af disse elektroner kræver mere energi på grund af den øgede tiltrækning.
3. Højeffektiv nuklear ladning: Den effektive nukleare ladning (Zeff) oplevet af valenselektroner i ædelgasser er højere end i halogener. Dette skyldes, at ædelgaskernen har en større positiv ladning, og der er færre indre elektroner til at skærme valenselektronerne fra kernen. Den stærkere tiltrækning mellem kernen og valenselektronerne gør det igen sværere at fjerne en elektron.
4. Fravær af elektronaffinitet: Halogener har en høj elektronaffinitet, hvilket betyder, at de let får en elektron for at opnå en stabil oktet. Det betyder, at de er mere tilbøjelige til at få en elektron i stedet for at miste en, hvilket resulterer i en lavere ioniseringsenergi sammenlignet med ædelgasser.
Opsummering:
* Ædelgasser er ekstremt stabile på grund af deres fulde valensskaller, hvilket resulterer i høje ioniseringsenergier.
* Den mindre størrelse og højere effektive nukleare ladning i ædelgasser bidrager yderligere til deres høje ioniseringsenergier.
I modsætning hertil får halogener let elektroner for at opnå stabilitet, hvilket gør deres ioniseringsenergi lavere end ædelgasser.
 Varme artikler
Varme artikler
-
 Afdækning af mikrogel-mysterierTC HS AFM-analyse af mikrogeler syntetiseret ved forskellige polymerisationsteknikker:(venstre) præcipitationspolymerisation, (i midten) invers miniemulsionspolymerisation under VPTT, og (højre) omven
Afdækning af mikrogel-mysterierTC HS AFM-analyse af mikrogeler syntetiseret ved forskellige polymerisationsteknikker:(venstre) præcipitationspolymerisation, (i midten) invers miniemulsionspolymerisation under VPTT, og (højre) omven -
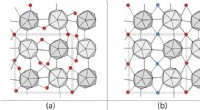 En ny opskrift til effektivt at fjerne iboende defekter fra hårde krystallerFigur 1. (a) Normal struktur af α-tetragonal bor. Mens icosaedre af bor (grå) har et ordnet atomarrangement, interstitielle boratomer (røde) er tilfældigt arrangeret. (b) Interstitielle atomer er arra
En ny opskrift til effektivt at fjerne iboende defekter fra hårde krystallerFigur 1. (a) Normal struktur af α-tetragonal bor. Mens icosaedre af bor (grå) har et ordnet atomarrangement, interstitielle boratomer (røde) er tilfældigt arrangeret. (b) Interstitielle atomer er arra -
 Undersøgelse demonstrerer tunbarheden af en molekylær chaperonePostdoc-forsker Wenli Meng, en ekspert i nuklear magnetisk resonansspektrometri i Gierasch Lab ved UMass Amherst, og kolleger udførte eksperimenter, der viste, at Hsp70er fra pattedyrsceller opfører s
Undersøgelse demonstrerer tunbarheden af en molekylær chaperonePostdoc-forsker Wenli Meng, en ekspert i nuklear magnetisk resonansspektrometri i Gierasch Lab ved UMass Amherst, og kolleger udførte eksperimenter, der viste, at Hsp70er fra pattedyrsceller opfører s -
 Klem stødet ud:Hvad forskellige faser af piezoelektriske materialer fortæller osForskere fra Gwangju Institut for Videnskab og Teknologi i Korea har undersøgt transformationsdynamikken induceret af et elektrisk felt i epitaksiale tyndfilm med blandet fase lanthanum-doteret bismut
Klem stødet ud:Hvad forskellige faser af piezoelektriske materialer fortæller osForskere fra Gwangju Institut for Videnskab og Teknologi i Korea har undersøgt transformationsdynamikken induceret af et elektrisk felt i epitaksiale tyndfilm med blandet fase lanthanum-doteret bismut
- Kan du forklare teorien om relativitet på enkle termer?
- Meroner realiseret i syntetiske antiferromagneter
- Hvorfor ændrer indikatorer i kemi farve, når de placeres forskellige stoffer?
- Hvad sker der, når du får en solskoldning?
- Syre-base reaktioner:Forståelse af oxid + vand reaktioner
- Hvad er grundene til udbredt brug af solenergi?


