Forståelse af ioniske bindinger:Dannelse og elektronegativitet
* Elektronegativitet: Dette er et mål for et atoms evne til at tiltrække elektroner i en kemisk binding.
* Stor forskel: Når det ene atom har en meget højere elektronegativitet end det andet, vil det mere elektronegative atom "stjæle" en elektron fra det mindre elektronegative atom. Dette resulterer i:
* Kationer: Atomet, der mister en elektron, bliver positivt ladet (fordi det nu har flere protoner end elektroner).
* Anioner: Atomet, der får en elektron, bliver negativt ladet (fordi det nu har flere elektroner end protoner).
* Elektrostatisk attraktion: De modsatte ladninger af kationen og anionen tiltrækker hinanden og danner ionbindingen.
Eksempler:
* Natriumchlorid (NaCl): Natrium (Na) har en lav elektronegativitet, mens klor (Cl) har en høj elektronegativitet. Klor tager en elektron fra natrium og danner en natriumion (Na+) og en chloridion (Cl-). Disse ioner tiltrækker derefter hinanden og danner ionbindingen i bordsalt.
* Magnesiumoxid (MgO): Magnesium (Mg) har en lavere elektronegativitet end oxygen (O). Oxygen tager to elektroner fra magnesium og danner en magnesiumion (Mg2+) og en oxidion (O2-). De modsatte ladninger tiltrækker og danner ionbindingen.
Nøglepunkter:
* Metaller og ikke-metaller: Ionbindinger dannes typisk mellem metaller (som har tendens til at miste elektroner) og ikke-metaller (som har tendens til at få elektroner).
* Gitterstruktur: Ionforbindelser danner krystalgitre, hvor kationerne og anionerne er arrangeret i et regelmæssigt, gentaget mønster. Denne struktur maksimerer den elektrostatiske tiltrækning mellem ionerne.
Lad mig vide, hvis du vil have flere eksempler eller en dybere forklaring af konceptet!
 Varme artikler
Varme artikler
-
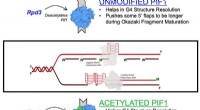 Kræftforbundet enzymmekanisme, der er nyligt karakteriseret i undersøgelseEt diagram, der illustrerer acetylering af Pif1-helicase-enzymet Kredit:Matthew Bochman og Lata Balakrishnan, Indiana University Bloomington/IUPUI En ny undersøgelse ledet af forskere ved IUPUI og
Kræftforbundet enzymmekanisme, der er nyligt karakteriseret i undersøgelseEt diagram, der illustrerer acetylering af Pif1-helicase-enzymet Kredit:Matthew Bochman og Lata Balakrishnan, Indiana University Bloomington/IUPUI En ny undersøgelse ledet af forskere ved IUPUI og -
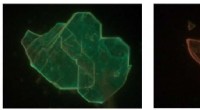 Kamæleonmaterialer:Oprindelsen af farvevariation i lavdimensionelle perovskitterBredfeltsfotoluminescensmikrofotografier (230_175 μm) viser, hvordan nogle Perovskite-flager ser lysegrønne ud over hele deres område (venstre panel), mens andre flager udviser en tydeligt rødforskudt
Kamæleonmaterialer:Oprindelsen af farvevariation i lavdimensionelle perovskitterBredfeltsfotoluminescensmikrofotografier (230_175 μm) viser, hvordan nogle Perovskite-flager ser lysegrønne ud over hele deres område (venstre panel), mens andre flager udviser en tydeligt rødforskudt -
 Passer én størrelse alle? En ny model for organiske halvledereRepræsentation af bærermobilitet i hårde uorganiske materialer (øverste figur, båndtransport) og fleksible organiske faste stoffer (nedre tal, fleksibilitetsinduceret transportmekanisme). Kredit:Kazuy
Passer én størrelse alle? En ny model for organiske halvledereRepræsentation af bærermobilitet i hårde uorganiske materialer (øverste figur, båndtransport) og fleksible organiske faste stoffer (nedre tal, fleksibilitetsinduceret transportmekanisme). Kredit:Kazuy -
 Kemisk dans af koboltkatalyse kan bane vej for solbrændstofferArgonne -kemikere Dugan Hayes, Lin Chen, og Ryan Hadt har identificeret en hurtig elektronisk proces, der kan hjælpe vandspaltningsreaktionen i koboltholdige katalysatorer. Koboltkatalysatorer er rela
Kemisk dans af koboltkatalyse kan bane vej for solbrændstofferArgonne -kemikere Dugan Hayes, Lin Chen, og Ryan Hadt har identificeret en hurtig elektronisk proces, der kan hjælpe vandspaltningsreaktionen i koboltholdige katalysatorer. Koboltkatalysatorer er rela
- Jordens nedre kappe kan oxideres i nærvær af vand
- Hvorfor mikroperler er sådan en trussel, og hvorfor de er så svære at håndtere
- Er der dybt akvifervand i Mojave -ørkenen?
- Når lille robot vil gå gennem dine værelser for at finde den orange pung
- Global gletsjersmeltning hæver havniveauet og udtømmer en gang pålidelig vandkilde
- Vil den rigtige Higgs Boson venligst rejse sig?


