Beregn Ksp af magnesiumhydroxid (Mg(OH)₂)
1. Skriv den balancerede opløsningsligning:
Mg(OH)₂(s) ⇌ Mg²⁺(aq) + 2OH⁻(aq)
2. Definer den molære opløselighed:
Den molære opløselighed (s) er koncentrationen af den opløste metalkation i en mættet opløsning. I dette tilfælde er s =1,4 x 10⁻⁴ M.
3. Udtryk ionkoncentrationerne i form af 's':
* [Mg²⁺] =s =1,4 x 10⁻⁴ M
* [OH⁻] =2s =2 * (1,4 x 10⁻4 M) =2,8 x 10⁻4 M
4. Skriv Ksp-udtrykket:
Ksp =[Mg²⁺][OH⁻]²
5. Udskift ionkoncentrationerne og beregn Ksp:
Ksp =(1,4 x 10⁻⁴ M)(2,8 x 10⁻⁴ M)²
Ksp =1,09 x 10⁻¹¹
Derfor er Ksp for magnesiumhydroxid 1,09 x 10⁻¹¹.
Sidste artikelForståelse af BTU-indhold i flydende naturgas (LNG)
Næste artikelBrom- og hydrogenreaktion:Kemisk ligning og forklaring
 Varme artikler
Varme artikler
-
 Spin-out-virksomhed hjælper med at få effektive lægemidler på markedet, hurtigere og billigereKredit:Swansea University At få bedre stoffer på markedet hurtigere, og til en brøkdel af prisen, er et skridt nærmere takket være teknologi til at fremskynde testprocessen, som udvikles af et spi
Spin-out-virksomhed hjælper med at få effektive lægemidler på markedet, hurtigere og billigereKredit:Swansea University At få bedre stoffer på markedet hurtigere, og til en brøkdel af prisen, er et skridt nærmere takket være teknologi til at fremskynde testprocessen, som udvikles af et spi -
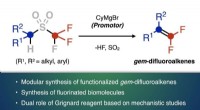 Etablering af en hurtig syntesemetode til nyttige organiske fluorforbindelserReaktionen af trifloner med det organiske magnesium-Grignard-reagens muliggør syntese af gem-difluoroalkenes Kredit:Issey Takahashi Nagoya University Institute of Transformative Bio-Molecules (W
Etablering af en hurtig syntesemetode til nyttige organiske fluorforbindelserReaktionen af trifloner med det organiske magnesium-Grignard-reagens muliggør syntese af gem-difluoroalkenes Kredit:Issey Takahashi Nagoya University Institute of Transformative Bio-Molecules (W -
 Genovervejelse af skadeproduktion og strålingsblanding i materialerTil venstre:Illustration af antallet af defekter i materialer forudsagt af den gamle Kinchin-Pease-ligning; Til højre:Illustration af det faktiske antal resterende skader, i overensstemmelse med forud
Genovervejelse af skadeproduktion og strålingsblanding i materialerTil venstre:Illustration af antallet af defekter i materialer forudsagt af den gamle Kinchin-Pease-ligning; Til højre:Illustration af det faktiske antal resterende skader, i overensstemmelse med forud -
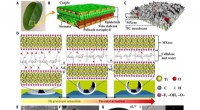 Bioinspireret MXene-baserede aktuatorer til programmerbare smartenhederDen udførlige struktur, komponenter, og aktiveringsmekanisme for den MXene-cellulosebaserede aktuator. (A) Fotografi af et naturligt blad. (B) Skematisk diagram af en bladstruktur. (C) Skematisk diagr
Bioinspireret MXene-baserede aktuatorer til programmerbare smartenhederDen udførlige struktur, komponenter, og aktiveringsmekanisme for den MXene-cellulosebaserede aktuator. (A) Fotografi af et naturligt blad. (B) Skematisk diagram af en bladstruktur. (C) Skematisk diagr


