Forståelse af syre- og basekoncentration:Molaritet vs. normalitet
Molaritet (M):
* Dette er den mest almindelige enhed, der bruges i kemi.
* Det repræsenterer antallet af mol opløst stof pr. liter opløsning.
* For eksempel indeholder en 1 M opløsning af saltsyre (HCl) 1 mol HCl pr. liter opløsning.
Normalitet (N):
* Denne enhed udtrykker antallet af ækvivalenter af opløst stof pr. liter opløsning.
* En ækvivalent er mængden af et stof, der kan reagere med eller erstatte ét mol hydrogenioner (H+) eller hydroxidioner (OH-).
* Normalitet bruges ofte til syrer og baser, fordi det er direkte relateret til antallet af mol H+ eller OH-ioner, der kan frigives i en reaktion.
Molalitet (m):
* Denne enhed repræsenterer antallet af mol opløst stof pr. kilogram opløsningsmiddel.
* Molalitet er mindre almindelig end molaritet, men er nyttig, når opløsningens volumen kan ændre sig med temperaturen, da opløsningsmidlets masse forbliver konstant.
Procentkoncentration:
* Denne enhed udtrykker mængden af opløst stof som en procentdel af den samlede opløsning.
* Der er flere variationer af procentkoncentration:
* Vægt/vægt (vægt/vægt): Gram opløst stof pr. 100 gram opløsning.
* Vægt/volumen (w/v): Gram opløst stof pr. 100 ml opløsning.
* Lydstyrke/Lydstyrke (v/v): Milliliter opløst stof pr. 100 ml opløsning.
pH:
* Denne enhed er et logaritmisk mål for hydrogenionkoncentrationen i en opløsning.
* Den går fra 0 til 14, med lavere pH-værdier, der indikerer højere surhedsgrad, og højere pH-værdier indikerer højere alkalinitet.
Den specifikke måleenhed, der anvendes, vil afhænge af konteksten og det ønskede præcisionsniveau. I de fleste tilfælde er molaritet (M) den mest almindelige og bekvemme enhed til at udtrykke koncentrationen af en syre eller base.
 Varme artikler
Varme artikler
-
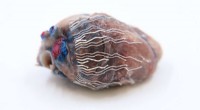 Tynd, strækbare biosensorer kan gøre operationen mere sikkerDe nye biosensorer giver mulighed for samtidig optagelse og billeddannelse af væv og organer under kirurgiske procedurer. På dette bilede, forskere fastgjorde biosensoren til hjertet af en gris, der b
Tynd, strækbare biosensorer kan gøre operationen mere sikkerDe nye biosensorer giver mulighed for samtidig optagelse og billeddannelse af væv og organer under kirurgiske procedurer. På dette bilede, forskere fastgjorde biosensoren til hjertet af en gris, der b -
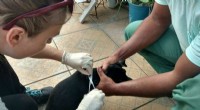 Elektronisk næse til at snuse hunde for dødelig tropesygdom i BrasilienTager hårprøver. Kredit:Lancaster University Færre hunde i Brasilien kan blive aflivet unødigt, efter at forskere har vist, at en ny test er 95 procent nøjagtig til at identificere den dødelige sy
Elektronisk næse til at snuse hunde for dødelig tropesygdom i BrasilienTager hårprøver. Kredit:Lancaster University Færre hunde i Brasilien kan blive aflivet unødigt, efter at forskere har vist, at en ny test er 95 procent nøjagtig til at identificere den dødelige sy -
 Teknik fordobler omdannelse af CO2 til plastkomponentMikroskopiske visninger af kobberskum når de ikke er behandlet (til venstre) vs. belagt med en polymer kaldet polyacrylamid, som ny forskning har vist, kan fordoble omdannelsen af C02 til ethylen. K
Teknik fordobler omdannelse af CO2 til plastkomponentMikroskopiske visninger af kobberskum når de ikke er behandlet (til venstre) vs. belagt med en polymer kaldet polyacrylamid, som ny forskning har vist, kan fordoble omdannelsen af C02 til ethylen. K -
 Forskere bruger sprogværktøjer til kunstig intelligens til at afkode molekylære bevægelserForskere fra University of Maryland anvendte et sprogbehandlingssystem til bevægelser af et riboswitchmolekyle afbildet her, at forstå, hvordan og hvornår molekylet antager forskellige former. Kredit:
Forskere bruger sprogværktøjer til kunstig intelligens til at afkode molekylære bevægelserForskere fra University of Maryland anvendte et sprogbehandlingssystem til bevægelser af et riboswitchmolekyle afbildet her, at forstå, hvordan og hvornår molekylet antager forskellige former. Kredit:
- Vigtigheden af foreløbig forskning i biologi:En omfattende vejledning
- Videnskaben sætter historiske påstande på prøve
- Hvilken type forskere var involveret i at opbygge Hubble -teleskopet?
- Den tilsyneladende stigende og nedgang af solen, som det ses fra Jorden, er forårsaget af?
- Omarrangering af det kemiske makeup -stof kaldes et hvad?
- Hvilken farve brænder natriumhydroxid i en flammetest?


