Ioniske vs. kovalente bindinger:Forstå de vigtigste forskelle
ioniske bindinger
* Formation: Ionbindinger dannes, når et atom *helt* overfører en eller flere elektroner til et andet atom. Denne overførsel skaber ioner:
* Kationer: Positivt ladede ioner dannes, når et atom mister elektroner.
* Anioner: Negativt ladede ioner dannes, når et atom får elektroner.
* Obligationens art: Den elektrostatiske tiltrækning mellem modsat ladede ioner holder dem sammen.
* Elektronegativitetsforskel: Ionbindinger opstår typisk mellem atomer med stor forskel i elektronegativitet (et atoms evne til at tiltrække elektroner).
* Ioniske forbindelsers egenskaber:
* Høje smelte- og kogepunkter: På grund af de stærke elektrostatiske kræfter.
* Fast ved stuetemperatur: De stærke kræfter holder ionerne i en stiv gitterstruktur.
* Gode ledere af elektricitet i smeltet eller opløst tilstand: Ionerne kan bevæge sig frit og bære elektrisk ladning.
* Skørt: Den stive gitterstruktur knækker let ved belastning.
Kovalente bindinger
* Formation: Kovalente bindinger dannes, når atomer *deler* et eller flere elektronpar.
* Obligationens art: De delte elektroner skaber et område med høj elektrontæthed, der tiltrækker de positivt ladede kerner i begge atomer og holder dem sammen.
* Elektronegativitetsforskel: Kovalente bindinger forekommer typisk mellem atomer med lignende eller små elektronegativitetsforskelle.
* Egenskaber af kovalente forbindelser:
* Lavere smelte- og kogepunkter: De svagere intermolekylære kræfter mellem molekyler fører til lettere adskillelse.
* Gasser, væsker eller faste stoffer ved stuetemperatur: Styrken af intermolekylære kræfter bestemmer deres fysiske tilstand.
* Dårlige ledere af elektricitet: Elektroner holdes tæt inde i de kovalente bindinger og flyder ikke frit.
Nøgleforskelle i en tabel:
| Funktion | Ionisk binding | Kovalent binding |
|---|---|---|
| Elektronoverførsel/deling | Fuldstændig overførsel | Deling |
| Resulterende ioner | Kationer og anioner | Ingen |
| Elektronegativitetsforskel | Stor | Lille eller ingen |
| Båndstyrke | Stærk | Relativt svagere |
| Ledningsevne | God i smeltet eller opløst tilstand | Dårlig |
| Smelte-/kogepunkt | Høj | Nedre |
Eksempler:
* Ionisk: Natriumchlorid (NaCl), Magnesiumoxid (MgO)
* Kovalent: Vand (H2O), Metan (CH4)
Vigtig bemærkning: I virkeligheden er der et spektrum af bindinger, og nogle bindinger har karakteristika for både ionisk og kovalent binding. Dette er kendt som polær kovalent binding .
 Varme artikler
Varme artikler
-
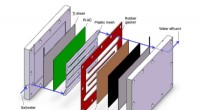 Ingeniører udvikler teknologi til at trække specifikke forurenende stoffer fra drikke- og spildeva…Rice Universitys nye platformsteknologi kan selektivt filtrere forurenende stoffer fra spildevand, drikkevand og industrivæsker. I test, en konstrueret belægning af harpiks, polymer og aktivt kul fjer
Ingeniører udvikler teknologi til at trække specifikke forurenende stoffer fra drikke- og spildeva…Rice Universitys nye platformsteknologi kan selektivt filtrere forurenende stoffer fra spildevand, drikkevand og industrivæsker. I test, en konstrueret belægning af harpiks, polymer og aktivt kul fjer -
 Forskning i havvands overfladespænding bliver international retningslinjeOverfladespænding er vandets egenskab, der gør det muligt for insekter at skumme vandoverfladen. Forskning udført af John Lienhard og Kishor Nayar for at forstå, hvordan havvandets overfladespænding æ
Forskning i havvands overfladespænding bliver international retningslinjeOverfladespænding er vandets egenskab, der gør det muligt for insekter at skumme vandoverfladen. Forskning udført af John Lienhard og Kishor Nayar for at forstå, hvordan havvandets overfladespænding æ -
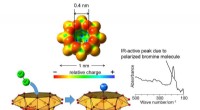 Polarisering af brommolekyle i vanadiumoxidklyngehulrum og ny alkanbromeringSpektrets top på grund af polariseret brommolekyle. Kredit:Kanazawa University Alkaner er hovedbestanddelene i naturgas og olie, kun bestående af kulstof- og brintatomer. CH-bindingerne af alkaner
Polarisering af brommolekyle i vanadiumoxidklyngehulrum og ny alkanbromeringSpektrets top på grund af polariseret brommolekyle. Kredit:Kanazawa University Alkaner er hovedbestanddelene i naturgas og olie, kun bestående af kulstof- og brintatomer. CH-bindingerne af alkaner -
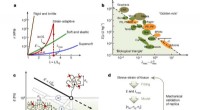 Kode til finjustering af elastomerer for at efterligne biologiske materialerProgrammering af mekanisk ydeevne. en, Den mekaniske mangfoldighed af biologiske og syntetiske materialer er illustreret ved enaksede trækspænding-deformationskurver, som afslører kombinationer af ege
Kode til finjustering af elastomerer for at efterligne biologiske materialerProgrammering af mekanisk ydeevne. en, Den mekaniske mangfoldighed af biologiske og syntetiske materialer er illustreret ved enaksede trækspænding-deformationskurver, som afslører kombinationer af ege
- Hvilket objekt ville have mindst acceleration, hvis du skubbede på det med en kraft på 6,5 N?
- Lærerrace og kønsbias:Opfattelser af elevernes tilgang til læring påvirker karakterer
- Hvordan spiser astronauter i rummet?
- Er der et videnskabeligt grundlag for horoskoper?
- Hvad gør en menneskelig celle?
- Hvad efterlod gamle mennesker sig for at fortælle os om månens sol og stjerner?


