Oxidationstal af H₂O:Forståelse af kemiske ladninger
Her er hvorfor:
* Oxidationstal repræsenterer den ladning et atom *ville* have, hvis alle bindingerne var ioniske. De er et bogføringsværktøj til at hjælpe os med at forstå elektronoverførsel i kemiske reaktioner.
* Oxidationstallet for et neutralt molekyle er altid 0.
Derfor er oxidationstallet for 6H2O 0 .
Men hvis du vil vide oxidationstallet for oxygenatomet i H₂O, er det -2. Dette skyldes, at brint typisk har et oxidationstal på +1 i forbindelser, og for at lave et neutralt H2O-molekyle skal oxygenet have en ladning -2.
 Varme artikler
Varme artikler
-
 Video:Sådan fungerer komposterbar plastKredit:The American Chemical Society På grund af miljøbevidste forbrugeres krav, producenter laver flere og flere engangsplastprodukter fra komposterbar polymælkesyre. Imidlertid, der er et par t
Video:Sådan fungerer komposterbar plastKredit:The American Chemical Society På grund af miljøbevidste forbrugeres krav, producenter laver flere og flere engangsplastprodukter fra komposterbar polymælkesyre. Imidlertid, der er et par t -
 Ammoniak:Et trumfkort til energiomstillingsprocessenKevin Rouwenhorst. Kredit:University of Twente Under sit praktikophold som Kemiteknologistuderende hos Haldor Topsøe, UT Ph.D. forsker Kevin Rouwenhorst indså de mange muligheder, som ammoniak give
Ammoniak:Et trumfkort til energiomstillingsprocessenKevin Rouwenhorst. Kredit:University of Twente Under sit praktikophold som Kemiteknologistuderende hos Haldor Topsøe, UT Ph.D. forsker Kevin Rouwenhorst indså de mange muligheder, som ammoniak give -
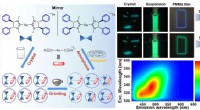 Forskere foreslår nye smarte selvlysende materialer af Au(I) dobbeltsalteFigur:Struktur af Au(I) dobbeltsalt (venstre) og luminescens under forskellig bølgelængde (højre). Kredit:CHEN Yong Smarte materialer, specielt til de dynamiske fysiske stimuli-responsive material
Forskere foreslår nye smarte selvlysende materialer af Au(I) dobbeltsalteFigur:Struktur af Au(I) dobbeltsalt (venstre) og luminescens under forskellig bølgelængde (højre). Kredit:CHEN Yong Smarte materialer, specielt til de dynamiske fysiske stimuli-responsive material -
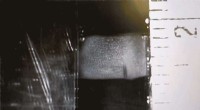 Syntetisk gelatine-lignende materiale efterligner jomfruhummers stræk og styrkeEn stålpartikel er vist, der trænger gennem den nanofibrøse hydrogel og forlader den med en reduceret hastighed. Forskellen i hastighed før og efter gav forskerne en direkte måling af materialets slag
Syntetisk gelatine-lignende materiale efterligner jomfruhummers stræk og styrkeEn stålpartikel er vist, der trænger gennem den nanofibrøse hydrogel og forlader den med en reduceret hastighed. Forskellen i hastighed før og efter gav forskerne en direkte måling af materialets slag


