Forståelse af pH-indikatorer:Hvordan de virker og farveændringer
Sådan fungerer indikatorer:
* Kemisk struktur: Indikatorer er normalt svage syrer eller baser med komplekse kemiske strukturer. De har forskellige farvede former alt efter om de er protonerede (har en brintion, H+) eller deprotonerede (har mistet en brintion).
* pH-følsomhed: Farveændringen i en indikator udløses af et skift i opløsningens pH (surhed eller alkalinitet).
* Ligevægt: I sure opløsninger er indikatormolekylet sandsynligvis protoneret, hvilket giver det én farve. I basisopløsninger vil molekylet sandsynligvis blive deprotoneret, hvilket giver det en anden farve.
Eksempler på indikatorer:
* Lakmuspapir: Bliver rød i sure opløsninger og blå i basiske opløsninger.
* Fenolphtalein: Farveløs i sure opløsninger og lyserød i basiske opløsninger.
* Methylorange: Rød i sure opløsninger og gul i basiske opløsninger.
* Bromthymol blå: Gul i sure opløsninger, grøn i neutrale opløsninger og blå i basiske opløsninger.
Beyond Indicators:
Mens indikatorer er de mest almindelige, kan andre stoffer også ændre farve i syrer eller baser, såsom:
* Nogle naturlige farvestoffer: Tænk på rødkålsjuice, som bliver rød i syre og blå i base.
* Visse metalioner: Opløsninger, der indeholder nogle metalioner, kan ændre farve afhængigt af pH.
Sig til, hvis du vil have flere oplysninger om en specifik indikator eller kemien bag deres farveændringer!
 Varme artikler
Varme artikler
-
 Forskere lærer mere om de første timer af et lithium-ion-batteris levetidForskere indlæser et specialdesignet lithium-ion-batteri i et sekundært ion-massespektrometer, der giver dem mulighed for at se dannelsen af fast-elektrolyt-interfasen på molekylært niveau, mens bat
Forskere lærer mere om de første timer af et lithium-ion-batteris levetidForskere indlæser et specialdesignet lithium-ion-batteri i et sekundært ion-massespektrometer, der giver dem mulighed for at se dannelsen af fast-elektrolyt-interfasen på molekylært niveau, mens bat -
 Metalindustrien er ved at gennemgå en af de største omvæltninger i historien, siger ekspertPotentielt bæredygtig:i dag, elektricitet bruges allerede til elektrolytisk udvinding af aluminium fra dets malme. I dag, elektricitet kommer ofte fra vandkraftværker, men også fra konventionelle kraf
Metalindustrien er ved at gennemgå en af de største omvæltninger i historien, siger ekspertPotentielt bæredygtig:i dag, elektricitet bruges allerede til elektrolytisk udvinding af aluminium fra dets malme. I dag, elektricitet kommer ofte fra vandkraftværker, men også fra konventionelle kraf -
 Kemikere opnår hidtil uset molekylært tredobbelthop med multi-ringede metalkomplekserTexas A&M Fremstående professor i kemi John A. Gladysz, forklarer den reaktionære mekanik involveret i et molekylært gyroskop. Kredit:Texas A&M University I årtier, Texas A&M University -kemiker D
Kemikere opnår hidtil uset molekylært tredobbelthop med multi-ringede metalkomplekserTexas A&M Fremstående professor i kemi John A. Gladysz, forklarer den reaktionære mekanik involveret i et molekylært gyroskop. Kredit:Texas A&M University I årtier, Texas A&M University -kemiker D -
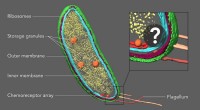 Ny teknik udpeger placeringer af individuelle molekyler i deres cellulære kvartererForskere fra Stanford University troede, at et tilsyneladende tomt område i den ene ende af Caulobacter-bakterien kunne indeholde to proteiner involveret i celledeling. Ved at mærke proteinerne med fl
Ny teknik udpeger placeringer af individuelle molekyler i deres cellulære kvartererForskere fra Stanford University troede, at et tilsyneladende tomt område i den ene ende af Caulobacter-bakterien kunne indeholde to proteiner involveret i celledeling. Ved at mærke proteinerne med fl
- Hvad kalder du tætheden af en elektronsky?
- Radioaktivt kulstof fra atombombe -test fundet i dybe havgrave
- Hvordan vil solen udvikle sig efter hovedstjernen?
- Opdagelse på et blomstergravsted kunne afsløre mysteriet om neandertaler-dødsritualer
- Hvordan er økosystemer og biomer forbundet?
- Hvad er tre vigtigste geografiske træk i Virginia?


