Salicylsyreopløselighed og saltsyre:En detaljeret forklaring
* Salicylsyre er en svag syre: Det eksisterer i ligevægt med dens konjugerede base, salicylation (C₇H5O3⁻).
* HCl er en stærk syre: Det ioniserer fuldstændigt i vand, hvilket giver en høj koncentration af H⁺-ioner.
* Le Chateliers princip: Når HCl tilsættes, flytter den høje koncentration af H⁺-ioner ligevægten af salicylsyreionisering til venstre . Dette betyder, at flere salicylsyremolekyler forbliver i deres udissocierede form, som er mindre opløseligt i vand.
Her er en forenklet forklaring:
1. Salicylsyre er delvist opløseligt i vand, fordi en lille mængde af den ioniseres og danner salicylationen (C₇H₅O₃⁻). Denne ion er mere polær og dermed mere opløselig i vand end det udissocierede salicylsyremolekyle.
2. Når HCl tilsættes, reagerer H+-ionerne fra HCl med salicylationerne og danner udissocieret salicylsyre. Dette reducerer koncentrationen af salicylationer i opløsning.
3. For at genetablere ligevægten vil flere salicylsyremolekyler skifte fra den opløste tilstand til den udissocierede form. Dette fører til et fald i den samlede opløselighed af salicylsyre.
Kort sagt undertrykker tilsætningen af HCl ioniseringen af salicylsyre, hvilket får mere af det til at forblive i sin mindre opløselige, udissocierede form.
 Varme artikler
Varme artikler
-
 Fra keglesneglegift til smertelindringDe kødædende havsnegle er kendt for deres forgiftningsmekanisme, som hjælper dyrene med at fange og forsvare deres bytte såsom fisk eller skaller. Kredit:Markus Muttenthaler Konotoksiner er bioakt
Fra keglesneglegift til smertelindringDe kødædende havsnegle er kendt for deres forgiftningsmekanisme, som hjælper dyrene med at fange og forsvare deres bytte såsom fisk eller skaller. Kredit:Markus Muttenthaler Konotoksiner er bioakt -
 Mineaffald kunne bruges som ingrediens til billigere brintbrændstofproduktionPulveriseret feltspat. Kredit:Dr. Hong Peng Forskere har opdaget en måde at bruge minedriftsaffald som en del af en potentiel billigere katalysator til produktion af brintbrændstof. Vandsplittend
Mineaffald kunne bruges som ingrediens til billigere brintbrændstofproduktionPulveriseret feltspat. Kredit:Dr. Hong Peng Forskere har opdaget en måde at bruge minedriftsaffald som en del af en potentiel billigere katalysator til produktion af brintbrændstof. Vandsplittend -
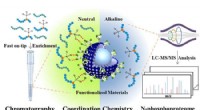 Forskere skræddersyr hurtig og effektiv N-phosphopeptides berigelsesstrategiBis (zink (II) -dipicolylamin) -funktionaliseret sub-2 μm core-shell mikrosfærer til analyse af N-phosphoproteom. Kredit:JIANG Bo og HU Yechen Protein N-phosphorylering spiller en kritisk rolle i
Forskere skræddersyr hurtig og effektiv N-phosphopeptides berigelsesstrategiBis (zink (II) -dipicolylamin) -funktionaliseret sub-2 μm core-shell mikrosfærer til analyse af N-phosphoproteom. Kredit:JIANG Bo og HU Yechen Protein N-phosphorylering spiller en kritisk rolle i -
 Selvstændig samling i flere trin åbner døren til nye rekonfigurerbare materialerMaterialevidenskab og ingeniørprofessor Qian Chen, centrum, og kandidatstuderende Binbin Luo, venstre, og Ahyoung Kim finder inspiration i biologi til at hjælpe med at undersøge, hvordan orden stammer
Selvstændig samling i flere trin åbner døren til nye rekonfigurerbare materialerMaterialevidenskab og ingeniørprofessor Qian Chen, centrum, og kandidatstuderende Binbin Luo, venstre, og Ahyoung Kim finder inspiration i biologi til at hjælpe med at undersøge, hvordan orden stammer
- Hvad er majsplastik?
- Undersøgelse:Hvordan studerende med forskellig baggrund bruger strategier til at styrke universitet…
- Urbach Tower tilbyder udsigt til selvformende arkitektur
- Hvad i alverden er vægt og højde på et objekt give hvilken type potentiel energi?
- Videospil kommer til Netflix? Seneste ansættelse giver et fingerpeg
- Titans søer kan stratificere som dem på Jorden


