Hastighedslov forklaret:Hvordan reaktantkoncentration påvirker reaktionshastigheden
Satslov:
```
Rate =k[A]^m[B]^n
```
hvor:
* Pris: Reaktionshastigheden, typisk målt i enheder af M/s (mol pr. liter pr. sekund).
* k: Hastighedskonstanten, en proportionalitetskonstant, der afspejler reaktionens iboende hastighed.
* [A] og [B] er koncentrationerne af henholdsvis reaktant A og B.
* m og n er rækkefølgen af reaktionen med hensyn til henholdsvis reaktant A og B. De er eksponenter bestemt eksperimentelt og angiver, hvordan hastigheden ændres med koncentrationen af hver reaktant.
Forklaring:
* Hastighedsloven siger, at hastigheden af en reaktion er direkte proportional med produktet af koncentrationerne af reaktanterne hævet til deres respektive rækkefølger.
* reaktionsrækkefølgen med hensyn til en specifik reaktant bestemmes eksperimentelt.
* Hvis ordren er 0 hastigheden er uafhængig af koncentrationen af den reaktant.
* Hvis ordren er 1 hastigheden er direkte proportional med koncentrationen af den reaktant.
* Hvis ordren er 2 , hastigheden er proportional med kvadratet af koncentrationen af den reaktant.
* Den overordnede rækkefølge af reaktionen er summen af de individuelle ordrer med hensyn til hver reaktant (m + n i dette tilfælde).
Eksempel:
Overvej reaktionen:
```
A + 2B → C
```
Hvis den eksperimentelt bestemte satslov er:
```
Rate =k[A]^1[B]^2
```
derefter:
* Reaktionen er første orden i forhold til A (m =1).
* Reaktionen er anden orden i forhold til B (n =2).
* Den overordnede rækkefølge af reaktionen er 3 (m + n =1 + 2).
Det betyder, at en fordobling af koncentrationen af A vil fordoble hastigheden, mens en fordobling af koncentrationen af B vil firdoble hastigheden.
 Varme artikler
Varme artikler
-
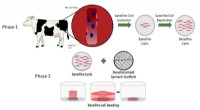 Decellulariseret spinat tjener som en spiselig platform for laboratoriedyrket kødDette diagram viser de trin, Boston College og WPI-forskere tog for at isolere og udså primære bovine satellitceller på et decellulariseret spinatbladstillads. Kredit:Food Bioscience Spinat, et om
Decellulariseret spinat tjener som en spiselig platform for laboratoriedyrket kødDette diagram viser de trin, Boston College og WPI-forskere tog for at isolere og udså primære bovine satellitceller på et decellulariseret spinatbladstillads. Kredit:Food Bioscience Spinat, et om -
 Ny katalysator med en dobbelt funktion til brint- og plastproduktionBochum -teamet:Dulce Morales, Steffen Cychy, Stefan Barwe, Dennis Hiltrop, Martin Muhler og Wolfgang Schuhmann (fra venstre). Kredit:RUB, Marquard Kemikere ved Ruhr-Universität Bochum (RUB) har ud
Ny katalysator med en dobbelt funktion til brint- og plastproduktionBochum -teamet:Dulce Morales, Steffen Cychy, Stefan Barwe, Dennis Hiltrop, Martin Muhler og Wolfgang Schuhmann (fra venstre). Kredit:RUB, Marquard Kemikere ved Ruhr-Universität Bochum (RUB) har ud -
 En ny brændselscelleelektrolytKredit:CC0 Public Domain Helt tilbage i 1930erne opfindere har kommercialiseret brændselsceller som en alsidig energikilde. Nu, forskere fra Japan har fremhævet den imponerende kemi af en væsentli
En ny brændselscelleelektrolytKredit:CC0 Public Domain Helt tilbage i 1930erne opfindere har kommercialiseret brændselsceller som en alsidig energikilde. Nu, forskere fra Japan har fremhævet den imponerende kemi af en væsentli -
 En unik kombination af katalysatorer åbner døre til fremstilling af nyttige forbindelserHuimin Zhao, Professor i kemisk og biomolekylær teknik ved University of Illinois i Urbana-Champaign Kredit:L. Brian Stauffer Forskere har udviklet en ny metode, der hjælper i processen med at fre
En unik kombination af katalysatorer åbner døre til fremstilling af nyttige forbindelserHuimin Zhao, Professor i kemisk og biomolekylær teknik ved University of Illinois i Urbana-Champaign Kredit:L. Brian Stauffer Forskere har udviklet en ny metode, der hjælper i processen med at fre
- Hvor kommer al energi på jorden fra?
- Da verden stoppede op for at se Armstrongs månevandring
- Hvilken slags binding er hydrogenperoxid?
- Hvorfor ser det ud til at blive varmere i skumringen?
- OECD-landenes politikere følger hinanden
- Hovedkomponenterne i biodiversitet, der forekommer inden for organismer på cellulært niveau, da de…


