pH vs. pOH:Forståelse af surhed og alkalinitet
* pH: Et mål for koncentrationen af hydrogenioner (H+) i en opløsning. En lavere pH betyder en højere koncentration af H+ ioner, hvilket indikerer surhedsgrad.
* pOH: Et mål for koncentrationen af hydroxidioner (OH-) i en opløsning. En lavere pOH betyder en højere koncentration af OH-ioner, hvilket indikerer alkalinitet.
Forholdet mellem pH og pOH:
* pH + pOH =14 (ved 25 grader Celsius)
Sådan bestemmer du, hvilken ion der er i højere koncentration:
* pH mindre end 7: Opløsningen er sur, hvilket betyder, at koncentrationen af H+-ioner er større end koncentrationen af OH-ioner.
* pH større end 7: Opløsningen er alkalisk (basisk), hvilket betyder, at koncentrationen af OH-ioner er større end koncentrationen af H+-ioner.
* pH lig med 7: Opløsningen er neutral, hvilket betyder, at koncentrationerne af H+ og OH- ioner er lige store.
Eksempel:
* En opløsning med en pH-værdi på 3 har en højere koncentration af H+-ioner end OH-ioner.
* En opløsning med en pOH på 11 har en højere koncentration af OH- ioner end H+ ioner.
Vigtig bemærkning: Udtrykkene "større koncentration" og "højere koncentration" er i det væsentlige udskiftelige i denne sammenhæng.
 Varme artikler
Varme artikler
-
 Takket være maskinlæring, fremtiden for katalysatorforskning er nu300 kvaternære katalysatorer udtages tilfældigt fra et stort materialerum, hvor deres ydeevne i forhold til OCM systematisk evalueres ved eksperimenter med høj gennemstrømning, efterfulgt af maskinlær
Takket være maskinlæring, fremtiden for katalysatorforskning er nu300 kvaternære katalysatorer udtages tilfældigt fra et stort materialerum, hvor deres ydeevne i forhold til OCM systematisk evalueres ved eksperimenter med høj gennemstrømning, efterfulgt af maskinlær -
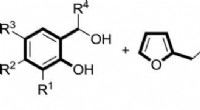 Russiske kemikere udviklede en måde at syntetisere stoffer fra vedvarende prækursorerDen nye enkle syntetiske vej til at opnå benzofuraner fra salicylalkoholer og N-tosylfurfurylamin. Kredit:Igor Trushkov Forskere fra RUDN University og deres russiske kolleger har udviklet en ny t
Russiske kemikere udviklede en måde at syntetisere stoffer fra vedvarende prækursorerDen nye enkle syntetiske vej til at opnå benzofuraner fra salicylalkoholer og N-tosylfurfurylamin. Kredit:Igor Trushkov Forskere fra RUDN University og deres russiske kolleger har udviklet en ny t -
 Sådan tilberedes en natriumkarbonatopløsning:En trin-for-trin guideAf bidragende skribent — Opdateret 24. marts 2022 Helmut Feil/iStock/GettyImages Natriumcarbonat (Na₂CO₃), almindeligvis kendt som vaskesodavand, er et uorganisk salt værdsat for dets alsidighed ind
Sådan tilberedes en natriumkarbonatopløsning:En trin-for-trin guideAf bidragende skribent — Opdateret 24. marts 2022 Helmut Feil/iStock/GettyImages Natriumcarbonat (Na₂CO₃), almindeligvis kendt som vaskesodavand, er et uorganisk salt værdsat for dets alsidighed ind -
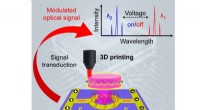 Ny rekord:3-D-printet optisk-elektronisk integrationSkematisk illustration af et integreret elektrisk styret mikrolasermodul til optoelektronisk hybridintegration. Kort, dette modul er designet til at være en termo-responsiv polymerresonator oven på et
Ny rekord:3-D-printet optisk-elektronisk integrationSkematisk illustration af et integreret elektrisk styret mikrolasermodul til optoelektronisk hybridintegration. Kort, dette modul er designet til at være en termo-responsiv polymerresonator oven på et


