Kovalente bindinger og vandopløselighed:Forståelse af forholdet
Kovalente bindinger i sig selv bestemmer ikke opløseligheden i vand. Det er *molekylet* dannet af de kovalente bindinger, der betyder noget.
Her er hvorfor:
* Vand er et polært molekyle: Vandmolekyler har en positiv ende (nær brintatomerne) og en negativ ende (nær iltatomet). Denne polaritet gør det muligt for vand at danne stærke hydrogenbindinger med andre polære molekyler.
* Polære molekyler opløses i vand: Når et polært molekyle som sukker (glukose) puttes i vand, omgiver vandmolekylerne sukkermolekylet og danner hydrogenbindinger med de polære grupper på sukkeret. Denne interaktion bryder sukkermolekylet fra hinanden og tillader det at opløses.
* Ikke-polære molekyler er uopløselige i vand: Ikke-polære molekyler, som olie, har ikke den samme polaritet. Vandmolekyler kan ikke danne stærke hydrogenbindinger med dem, så de forbliver adskilte og opløses ikke.
Så opløseligheden af en kovalent forbindelse i vand afhænger af dens samlede polaritet:
* Polære kovalente molekyler: Disse molekyler har en ujævn fordeling af elektroner, hvilket skaber partielle ladninger. De er *opløselige* i vand, fordi de kan danne brintbindinger med vandmolekyler. Eksempler:sukker, ethanol.
* Ikke-polære kovalente molekyler: Disse molekyler har en jævn fordeling af elektroner, hvilket fører til ingen partielle ladninger. De er *uopløselige* i vand, fordi de ikke kan danne brintbindinger med vandmolekyler. Eksempler:olie, metan.
Nøgleafhentning: Det er ikke selve den kovalente binding, men *polariteten* af molekylet skabt af bindingen, der dikterer opløseligheden i vand.
Sidste artikelSammensætning af jernoxid:Jern og ilt
Næste artikelCobalt(VI)chlorid:hvorfor det ikke eksisterer og kemisk stabilitet
 Varme artikler
Varme artikler
-
 Rød eller gul? En simpel papirtest afslører falske eller substandard antibiotikaEn enkel, papirbaseret test kan hurtigt identificere et forfalsket eller substandard antibiotikum. Kredit:John Eisele/Colorado State University Antibiotika – medicin, der behandler bakterielle inf
Rød eller gul? En simpel papirtest afslører falske eller substandard antibiotikaEn enkel, papirbaseret test kan hurtigt identificere et forfalsket eller substandard antibiotikum. Kredit:John Eisele/Colorado State University Antibiotika – medicin, der behandler bakterielle inf -
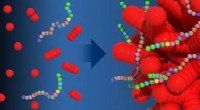 Koralformede nanopartikler bygget af design ved hjælp af konstruerede peptoiderI en ny undersøgelse ledet af PNNL-materialeforsker Chun-Long Chen, sekvensdefinerede peptoider (vist her som kæder af små farverige kugler) muliggjorde den forudsigelige morfologiske udvikling af sfæ
Koralformede nanopartikler bygget af design ved hjælp af konstruerede peptoiderI en ny undersøgelse ledet af PNNL-materialeforsker Chun-Long Chen, sekvensdefinerede peptoider (vist her som kæder af små farverige kugler) muliggjorde den forudsigelige morfologiske udvikling af sfæ -
 Fysik kontra astmaSegmenterne i CysLT1 -receptoren, der er ansvarlig for dets aktivering, er vist i orange, ved siden af andre G-proteinkoblede receptorer. Kredit:Luginina et al./Science Advances Et forskerhold f
Fysik kontra astmaSegmenterne i CysLT1 -receptoren, der er ansvarlig for dets aktivering, er vist i orange, ved siden af andre G-proteinkoblede receptorer. Kredit:Luginina et al./Science Advances Et forskerhold f -
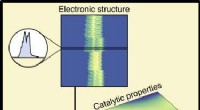 Maskinlæring forbinder materialesammensætning og ydeevne i katalysatorerKredit:University of Michigan I et fund, der kunne være med til at bane vejen mod renere brændstoffer og en mere bæredygtig kemisk industri, forskere ved University of Michigan har brugt maskinlær
Maskinlæring forbinder materialesammensætning og ydeevne i katalysatorerKredit:University of Michigan I et fund, der kunne være med til at bane vejen mod renere brændstoffer og en mere bæredygtig kemisk industri, forskere ved University of Michigan har brugt maskinlær
- Stoffer, der kan omdannes til en gas ved relativt lave temperaturer, kaldes?
- Downloader af walkie-talkie-apps stiger, når Irma vælder
- Hvad er de vigtige komponenter i et eksperiment?
- Hvilket land ligger ved 75 grader nord og 120 vest?
- Microsoft afdækker mere russisk hacking forud for midterms
- Amerikanerne foretrækker økonomisk ulighed frem for at spille Robin Hood, undersøgelse finder


