Opløsning vs. reaktion i vand:en klar skelnen
Opløser
* Der dannes ingen nye stoffer. Det faste stof nedbrydes simpelthen til dets individuelle ioner eller molekyler, som derefter er omgivet af vandmolekyler.
* Processen er normalt reversibel. Du kan ofte genvinde det oprindelige faste stof ved at fordampe vandet.
* Der produceres ingen gas.
* Ingen ændring i temperatur (eller en meget lille, ubetydelig ændring).
Reagerer
* Nye stoffer dannes. Det originale faste stof kombineres kemisk med vandmolekyler og skaber nye forbindelser.
* Processen er normalt ikke let reversibel. Du vil ikke være i stand til at få det originale faste stof tilbage ved blot at fordampe vandet.
* Gas kan produceres.
* Der er en mærkbar ændring i temperaturen. Opløsningen kan blive varmere (exoterm reaktion) eller koldere (endoterm reaktion).
Eksempler:
* Opløsning: Salt (NaCl) opløses i vand. Saltet nedbrydes til Na+ og Cl-ioner, men selve saltets kemiske sammensætning har ikke ændret sig. Du kan få saltet tilbage ved at fordampe vandet.
* Reagerer: Natriummetal (Na) reagerer med vand. Dette producerer natriumhydroxid (NaOH) og hydrogengas (H2). Natriumet har kemisk reageret med vand for at danne nye stoffer. Du kan ikke bare få natriumet tilbage ved at fordampe vandet.
Praktiske observationer:
* Udseende: Forsvinder det faste stof helt ud i vandet, eller ser du nogen synlige ændringer i opløsningen (farveændring, uklarhed)?
* Opvarmning/køling: Føles opløsningen varmere eller koldere, efter at det faste stof er opløst?
* Gasproduktion: Kan du se, at der dannes bobler?
* Lugt: Har opløsningen en ny, tydelig lugt, efter at det faste stof er opløst?
Vigtig bemærkning: Nogle gange kan det være svært at kende forskel på at opløse og reagere. Hvis du er usikker, er det altid bedst at konsultere en pålidelig kilde til kemisk information.
Sidste artikelEn historie om giftgas:oprindelse og udvikling
Næste artikelBeregning af FeCl3-koncentration:En trin-for-trin guide
 Varme artikler
Varme artikler
-
 Gnisten der skabte livEvolution ved naturlig udvælgelse er uhyre stærk - både i naturen og i laboratorier. Forskere har identificeret strukturelle kapacitanselementer i proteiner, som bevarer potentialet til at udvikle sig
Gnisten der skabte livEvolution ved naturlig udvælgelse er uhyre stærk - både i naturen og i laboratorier. Forskere har identificeret strukturelle kapacitanselementer i proteiner, som bevarer potentialet til at udvikle sig -
 Forskningsteam afdækker ekstraordinære egenskaber ved strontiumniobatForskere ledet af professor T Venky Venkatesan (første række, centrum), Direktør for NUSNNI, afdækkede ekstraordinære egenskaber ved halvledermateriale strontiumniobat. Kredit:National University of S
Forskningsteam afdækker ekstraordinære egenskaber ved strontiumniobatForskere ledet af professor T Venky Venkatesan (første række, centrum), Direktør for NUSNNI, afdækkede ekstraordinære egenskaber ved halvledermateriale strontiumniobat. Kredit:National University of S -
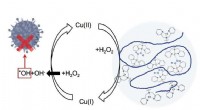 Ny strategi for lægemiddeldesign:At holde kobberatomer tættere på for at holde bakterier vækDen foreslåede polymer, med rygraden vist i blåt, skaber regioner med en høj lokal densitet af kobbersideenheder (vedhæng). Dette hjælper med at reducere Cu (II) til Cu (I), det vanskeligste trin i re
Ny strategi for lægemiddeldesign:At holde kobberatomer tættere på for at holde bakterier vækDen foreslåede polymer, med rygraden vist i blåt, skaber regioner med en høj lokal densitet af kobbersideenheder (vedhæng). Dette hjælper med at reducere Cu (II) til Cu (I), det vanskeligste trin i re -
 Flydende krystallers overraskende styrkeForskere er et skridt tættere på at udvikle længerevarende og sikrere batterier ved hjælp af flydende krystaller. Kredit:Pixabay Dendritter er de ødelæggende biprodukter af cyklussen med opladning
Flydende krystallers overraskende styrkeForskere er et skridt tættere på at udvikle længerevarende og sikrere batterier ved hjælp af flydende krystaller. Kredit:Pixabay Dendritter er de ødelæggende biprodukter af cyklussen med opladning


