Magnesium og svovl:Forståelse af dannelsen af en ionisk binding
* Forskel på elektronegativitet: Magnesium har en lav elektronegativitet (1,31), mens svovl har en højere elektronegativitet (2,58). Denne signifikante forskel i elektronegativitet (1,27) indikerer en stærk tendens for svovl til at tiltrække elektroner fra magnesium.
* Elektronkonfiguration:
* Magnesium (Mg) har to valenselektroner i sin ydre skal. Den mister let disse to elektroner for at opnå en stabil oktetkonfiguration som ædelgassen neon (Ne).
* Svovl (S) har seks valenselektroner. Den har brug for to elektroner mere for at opnå en stabil oktetkonfiguration som ædelgassen argon (Ar).
* Danning af ioner:
* Magnesium mister sine to valenselektroner og bliver til en positivt ladet ion (Mg²⁺).
* Svovl får to elektroner til at blive en negativt ladet ion (S²⁻).
* Elektrostatisk tiltrækning:
* De modsat ladede ioner (Mg²⁺ og S²⁻) tiltrækker hinanden på grund af elektrostatiske kræfter og danner en ionbinding.
Resultatet:
Den stærke elektrostatiske tiltrækning mellem de positivt ladede magnesiumioner (Mg²⁺) og de negativt ladede sulfidioner (S²⁻) resulterer i dannelsen af en ionisk forbindelse, magnesiumsulfid (MgS).
 Varme artikler
Varme artikler
-
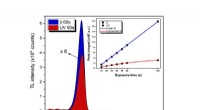 Aluminiumoxidkrystal testet som UV-strålingssensorIntensitet og temperatur. Detektering og måling af UV-eksponering i forskellige miljøer var omfanget af en undersøgelse. Kredit:Neilo Marcos Trindade og hans team Udsættelse for ultraviolet (UV) s
Aluminiumoxidkrystal testet som UV-strålingssensorIntensitet og temperatur. Detektering og måling af UV-eksponering i forskellige miljøer var omfanget af en undersøgelse. Kredit:Neilo Marcos Trindade og hans team Udsættelse for ultraviolet (UV) s -
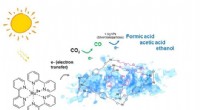 Ny lysaktiveret katalysator fanger CO2 for at lave ingredienser til brændstofSkematisk af en svampet nikkel-organisk fotokatalysator, der udelukkende omdanner carbondioxid til carbonmonoxid, som yderligere kan omdannes til flydende brændstof af høj værdi gennem synlig lys-indu
Ny lysaktiveret katalysator fanger CO2 for at lave ingredienser til brændstofSkematisk af en svampet nikkel-organisk fotokatalysator, der udelukkende omdanner carbondioxid til carbonmonoxid, som yderligere kan omdannes til flydende brændstof af høj værdi gennem synlig lys-indu -
 Forskere finder, at frøskal kunne føre til stærke, hård, men alligevel fleksible materialerKarakteristiske træk ved frøkappen af Portulaca oleracea , en årlig sukkulent almindeligvis kendt som verdolaga eller portulak. A) Foto af P. oleracea blomst , B) Fotografi af de bittesmå sorte fr
Forskere finder, at frøskal kunne føre til stærke, hård, men alligevel fleksible materialerKarakteristiske træk ved frøkappen af Portulaca oleracea , en årlig sukkulent almindeligvis kendt som verdolaga eller portulak. A) Foto af P. oleracea blomst , B) Fotografi af de bittesmå sorte fr -
 Kuldioxidmineralisering i geologisk almindelige bjergarter til kulstoflagringDen røde farve angiver, at sandsynligheden for forekomst af valenselektroner er 100 procent, den blå farve betyder, at der ikke findes elektroner i området, og den grønne farve betyder fri elektrongas
Kuldioxidmineralisering i geologisk almindelige bjergarter til kulstoflagringDen røde farve angiver, at sandsynligheden for forekomst af valenselektroner er 100 procent, den blå farve betyder, at der ikke findes elektroner i området, og den grønne farve betyder fri elektrongas
- Monobasiske syrer:eksempler, egenskaber og anvendelser
- Selv hvis TikTok og andre apps indsamler dine data, hvad er så de faktiske konsekvenser?
- Hvordan reagerer jordskorpen på tilføjelse og subtraktion af masse?
- Facilitering af en smidig teknologisk overgang for borgere, der vender tilbage fra fængslet
- Tsunamien udløst af Anak Krakatoa-udbruddet var mindst 100 meter høj
- Rakettestopsendelse for Space Force når ikke i kredsløb


