Elektronegativitetsrangering:Svovl, Oxygen, Neon, Aluminium - Forklaret
Forståelse af elektronegativitet
Elektronegativitet er et mål for et atoms evne til at tiltrække elektroner i en kemisk binding. Jo højere elektronegativitet, jo stærkere er træk.
Tendenser inden for elektronegativitet
* Øger over en periode (fra venstre mod højre): Atomer i samme periode har det samme antal elektronskaller, men når man bevæger sig hen over perioden, stiger antallet af protoner i kernen. Denne stærkere positive ladning trækker elektronerne tættere på, hvilket gør dem sværere at fjerne.
* Reducerer en gruppe ned (fra top til bund): Når du bevæger dig ned ad en gruppe, bliver elektronskallerne større. De yderste elektroner er længere væk fra kernen, og tiltrækningen er svagere.
Rangering af elementerne
1. Neon (Ne): Neon er en ædelgas, hvilket betyder, at den har en fuld ydre skal af elektroner. Den har en meget lav elektronegativitet, fordi den ikke behøver at få flere elektroner.
2. Aluminium (Al): Aluminium er et metal, og metaller har en tendens til at have lavere elektronegativitet end ikke-metaller. Den er placeret i gruppe 13, så dens elektronegativitet er relativt lav.
3. Svovl (S): Svovl er et ikke-metal, og ikke-metaller har generelt højere elektronegativitet end metaller. Den er placeret i gruppe 16, hvilket betyder, at den har et stærkere træk på elektroner end aluminium.
4. Oxygen (O): Ilt er også et ikke-metal og er i gruppe 16. Det er dog placeret højere oppe i gruppen end svovl, hvilket gør det mere elektronegativt.
Endelig rangering (øgende elektronegativitet)
1. Neon (Ne)
2. Aluminium (Al)
3. Svovl (S)
4. Ilt (O)
 Varme artikler
Varme artikler
-
 Den eukaryote cellekerne ligner layoutet af en superbutikHylder stående i supermarkedet er adskilt med gange, så folk nemt kan krydse hver gang, når de handler. Kernen fungerer som superbutikken, hvor i stedet for hylder, der er kromatinfibre. Disse fibre h
Den eukaryote cellekerne ligner layoutet af en superbutikHylder stående i supermarkedet er adskilt med gange, så folk nemt kan krydse hver gang, når de handler. Kernen fungerer som superbutikken, hvor i stedet for hylder, der er kromatinfibre. Disse fibre h -
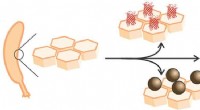 Engineering levende stilladser til byggematerialerBerkeley Lab -forskere byggede et sæt bakterier, der irreversibelt kan vedhæfte en række hårde eller bløde materialer som biopolymerer eller halvledende nanopartikler til celleoverfladen uden at beska
Engineering levende stilladser til byggematerialerBerkeley Lab -forskere byggede et sæt bakterier, der irreversibelt kan vedhæfte en række hårde eller bløde materialer som biopolymerer eller halvledende nanopartikler til celleoverfladen uden at beska -
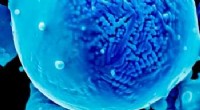 Tilpasning af legeringens mikrokemi til fejlfri metal 3D -printEn ny metode udviklet af Texas A&M-forskere optimerer legeringsegenskaber og procesparametre til at skabe overlegne 3D-printede metaldele. Her er vist et farvet elektronmikrograf af en nikkelpulverleg
Tilpasning af legeringens mikrokemi til fejlfri metal 3D -printEn ny metode udviklet af Texas A&M-forskere optimerer legeringsegenskaber og procesparametre til at skabe overlegne 3D-printede metaldele. Her er vist et farvet elektronmikrograf af en nikkelpulverleg -
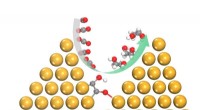 Super-selektive katalysatorer er nøglen til kulstofomdannelseDen unikke rumlige indeslutning induceret af kobbernanopyramider er afgørende for selektivt at generere ethylenglycol gennem en ny reaktionsvej. Kredit:Shizhang Qiao, Universitetet i Adelaide Kata
Super-selektive katalysatorer er nøglen til kulstofomdannelseDen unikke rumlige indeslutning induceret af kobbernanopyramider er afgørende for selektivt at generere ethylenglycol gennem en ny reaktionsvej. Kredit:Shizhang Qiao, Universitetet i Adelaide Kata
- Forsker trækker fra fortid for at forme fremtiden for glasforskning
- Bærbart miljøkammer licenseret til FOM-teknologier
- Kan klimaændringer skabe en helt ny kategori af orkaner?
- AI-kornvurdering sår frø for bedre afkast
- Undersøgelse af fritfaldende papirformer kan hjælpe med at designe bio-inspireret robotik
- Hvad er 50 nanogrammer?


