Natriumchloridopløselighed og farve i forskellige opløsningsmidler:en detaljeret forklaring
* Natriumchlorid (NaCl) i vand: NaCl opløses let i vand og danner en klar, farveløs opløsning. Dette skyldes, at vand er et polært opløsningsmiddel, og NaCl er en ionisk forbindelse, hvilket betyder, at det let dissocieres til positivt ladede natriumioner (Na+) og negativt ladede chloridioner (Cl-) i vand.
* Natriumchlorid i ethanol: Ethanol er også et polært opløsningsmiddel, men mindre polært end vand. Mens NaCl vil opløses i ethanol til en vis grad, vil det være meget mindre opløseligt end i vand. Opløsningen vil fremstå klar og farveløs.
* Natriumchlorid i chloroform: Chloroform er et ikke-polært opløsningsmiddel. NaCl er ikke opløseligt i chloroform. Du vil se to forskellige lag:den tættere chloroform i bunden og NaCl i toppen.
Nøgleudtag: Natriumchlorid er mest opløseligt i polære opløsningsmidler som vand. Dens opløselighed falder i mindre polære opløsningsmidler som ethanol og er praktisk talt ikke-eksisterende i ikke-polære opløsningsmidler som chloroform. Farven forbliver uændret i alle disse tilfælde, da NaCl selv er farveløs.
 Varme artikler
Varme artikler
-
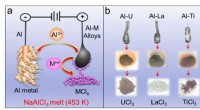 Forskere foreslår IAP-proces til adskillelse af aluminiumslegeringerFigur:IAP-proces. (a) Skematisk illustration af IAP-processen i NaAlCl4-smeltet saltelektrolyt. (b) Forskellige legeringer og tilsvarende metalchlorider udfældet i bunden af digelen ved elektrolyse
Forskere foreslår IAP-proces til adskillelse af aluminiumslegeringerFigur:IAP-proces. (a) Skematisk illustration af IAP-processen i NaAlCl4-smeltet saltelektrolyt. (b) Forskellige legeringer og tilsvarende metalchlorider udfældet i bunden af digelen ved elektrolyse -
 Udvidelse af rækkevidden af terapeutiske antistofferEt enkelt bispecifikt antistof kan binde til flere antigener, resulterer i mere specifik målretning, nye virkningsmekanismer og højere klinisk effektivitet. Kredit:Camilla De Nardis, Linda J.A. Hendri
Udvidelse af rækkevidden af terapeutiske antistofferEt enkelt bispecifikt antistof kan binde til flere antigener, resulterer i mere specifik målretning, nye virkningsmekanismer og højere klinisk effektivitet. Kredit:Camilla De Nardis, Linda J.A. Hendri -
 Gennembrud i at udnytte kraften fra biologiske katalysatorerForskningen er et skridt i retning af at integrere enzymer i den nuværende kemiske industriinfrastruktur. Kredit:University of Bath Naturens kraft kan snart bruges til at skabe daglige materialer
Gennembrud i at udnytte kraften fra biologiske katalysatorerForskningen er et skridt i retning af at integrere enzymer i den nuværende kemiske industriinfrastruktur. Kredit:University of Bath Naturens kraft kan snart bruges til at skabe daglige materialer -
 Fremstilling af etan fra metan ved hjælp af en fotokemisk looping -strategiÆndringer af Ag – HPW/TiO 2 efter metan fotokemisk kobling. Kredit: Naturenergi (2020). DOI:10.1038/s41560-020-0616-7 Et team af forskere fra universitetet i Lille, CNRS, Centrale Lille, Univer
Fremstilling af etan fra metan ved hjælp af en fotokemisk looping -strategiÆndringer af Ag – HPW/TiO 2 efter metan fotokemisk kobling. Kredit: Naturenergi (2020). DOI:10.1038/s41560-020-0616-7 Et team af forskere fra universitetet i Lille, CNRS, Centrale Lille, Univer
- En ligevægtsblanding indeholder n2o4 p er lig med 0,30 ATM og no2 1,1atm ved 350 k volumen af beh…
- Raket klingende vil tage 1, 500 billeder af sol på fem minutter
- Sådan genbruger hajer giftig ammoniak for at holde deres hud fugtig
- Hvordan adskiller receptormedieret endocytose sig fra lettet diffusion?
- Hvilket af disse er et eksempel et sammensat jern eller kuldioxidoxygencalcium?
- Hvordan konverterer turbinen kinetisk energi til elektrisk energi?


