Udvidelse af rækkevidden af terapeutiske antistoffer
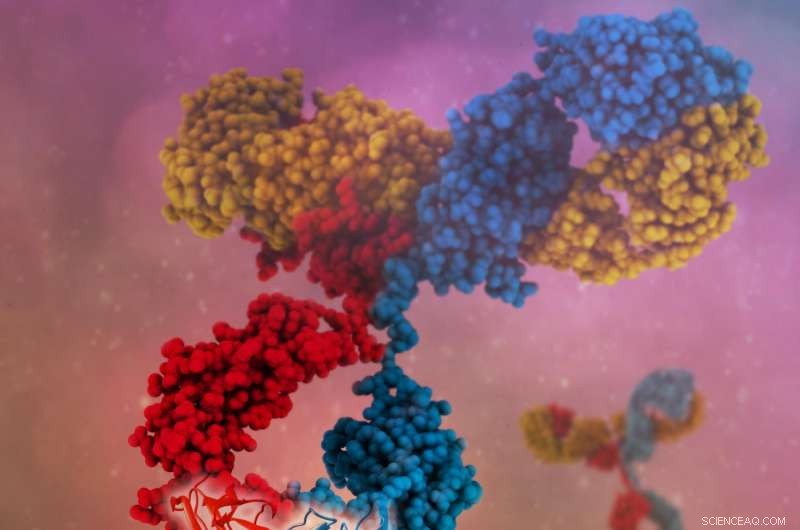
Et enkelt bispecifikt antistof kan binde til flere antigener, resulterer i mere specifik målretning, nye virkningsmekanismer og højere klinisk effektivitet. Kredit:Camilla De Nardis, Linda J.A. Hendriks, Emilie Poirier, Tudor Arvinte, Piet Gros, Alexander B. H. Bakker og John de Kruif
En gruppe forskere har udviklet en tilgang til effektivt at producere antistoffer, der kan binde til to forskellige målmolekyler samtidigt, en længe ønsket innovation inden for kræftimmunterapi. Detaljerne vil blive offentliggjort i 1. september -udgaven af Journal of Biological Chemistry .
Antistoffer er proteiner produceret af immunsystemet, der er specialiseret i at genkende og binde sig til molekylære mål, der er unikke for bakterier, vira eller andre fremmede celler. Fordi antistoffer er stabile og langvarige i den menneskelige krop og præcist kan genkende specifikke mål, de er blevet udnyttet til at udvikle nye behandlinger for sygdomme. For eksempel, modificerede antistoffer kan bruges til at binde sig til mål i kræftceller, rekruttere immunsystemet til at angribe kræften eller forhindre kræftcellerne i at formere sig. På grund af deres præcision og evne til at stimulere kroppens immunrespons, antistof-baserede terapier har typisk færre bivirkninger end kemoterapi eller stråling.
Antistoffer er "Y" formet, og binder typisk et mål, eller antigen, gennem spidsen af hver arm af "Y". I naturligt producerede antistoffer, begge arme af et enkelt antistof er typisk de samme og binder til det samme mål. En tilgang til at øge alsidigheden af antistofterapier er at konstruere det, der kaldes bispecifikke antistoffer, hvor hver arm binder sig til et forskelligt molekyle. Dette udvider rækkevidden af hvad antistoffer kan bruges til. For eksempel, et bispecifikt antistof kunne målrette mod en klynge af proteiner, der består af flere proteintyper, eller det kunne bringe to forskellige molekyler eller celletyper sammen.
Et bispecifikt antistoflignende lægemiddel - leukæmilægemidlet blinatumomab - er i øjeblikket på markedet. Men udviklingen af flere terapier baseret på bispecifikke antistoffer er blevet hæmmet af tekniske udfordringer. For eksempel, visse bispecifikke antistoffer afviger fra standard Y-formen og har tendens til at være mindre stabile end konventionelle antistoffer, falder let fra hinanden. Yderligere, visse bispecifikke antistofformater har haft en tendens til at være vanskelige at fremstille i industriel skala, fordi de kan kræve specialiserede ingeniørprocesser.
I eksperimenter offentliggjort i JBC, et team under opsyn af John de Kruif, teknologichefen for forskningsvirksomheden Merus N.V. i klinisk fase, konstrueret forbedrede bispecifikke antistoffer ved at foretage nogle få vigtige ændringer i strukturen af naturlige humane immunglobulin G (IgG) antistoffer, og viste, at de let kunne fremstilles. IgG er et velundersøgt antistof og er det mest udbredte, der produceres i den menneskelige krop.
"Vi har lavet, i et komplet IgG-molekyle, kun fire ændringer for at gå fra et normalt monospecifikt antistof til bispecifikt antistof, " sagde de Kruif. "Det fantastiske er, at det ligner så meget et normalt antistof, at vi kan producere det godt, og vi tror, vi ved, hvordan det vil opføre sig."
De fire mutationer var i "tung kæde"-proteinkomponenterne i antistofferne. Typisk, to identiske tunge kæder parrer sig i hvert antistof. Udfordringen med at skabe bispecifikke antistoffer var at inducere ikke-identiske tunge kæder til at parre - skabe "arme", der er i stand til at binde forskellige antigener - samtidig med at man fraråder parring af identiske.
Holdets idé var at introducere aminosyrer med modsatte ladninger til de to forskellige tunge kæder, således at identiske tunge kæder ville frastøde hinanden, hvorimod de positivt og negativt ladede tunge kæder ville tiltrække. For at identificere de rigtige steder at indføre disse gebyrer, de brugte beregningssimuleringer ved hjælp af virtuel screeningssoftware efterfulgt af validering i laboratoriet.
"Ved brug af den virtuelle screeningssoftware gav en baseline, " sagde Linda Kaldenberg-Hendriks fra Merus, som ledede testningen af antistofferne. "Vi identificerede potentielle gode kandidater til designvalg i de tunge kædesæt, genererede derefter proteinerne og karakteriserede dem grundigt. Da vi så, at de opførte sig, som vi ville have dem til, det var virkelig tilfredsstillende."
Holdet undersøgte også den molekylære struktur af de bispecifikke antistoffer, og bekræftede, at mutationerne kun resulterede i meget subtile ændringer i "rygraden" af de tunge kæder, hvilket kan forklare stabiliteten af disse bispecifikke antistoffer.
"En stærk pointe [af denne undersøgelse] var at kombinere forskellige tilgange, de beregningsmæssige værktøjer med biokemi og strukturel biologi, " sagde Camilla De Nardis fra Merus og Utrecht University, som var medforfatter på undersøgelsen.
De proteiner, der virkede, blev parret til dannelse af bispecifikke antistoffer, med meget få eller ingen monospecifikke antistoffer i blandingen. Holdet udsatte dem derefter for en række tests, bekræfter, at de var lige så stabile som normale IgG -antistoffer og havde lignende farmakokinetiske egenskaber.
Fordi produktion og oprensning af IgG-antistoffer er en veletableret industriel proces, holdet kunne simpelthen give producenterne proteinsekvenserne modificeret med de vigtigste ændringer, der gjorde det muligt for proteinerne at danne bispecifikke. "Vi tror på, at vi kan lave stort set ethvert bispecifikt antistof, vi ønsker, "Sagde Kaldenberg-Hendriks.
Holdets bispecifikke antistoffer rettet mod kræftcellevækstfaktorkomplekser er nu i kliniske forsøg, med mere stadig i den prækliniske pipeline. Teamet er begejstret for potentialet for, at det alsidige format kan tilpasses forskellige typer terapier.
"Antistoffer er i stand til at være så specifikke, og du kan justere og justere dem, " sagde Kaldenberg-Hendriks. "Med bispecifikke antistoffer, vi tror på, at vi kan vælge affiniteterne af begge arme og afbalancere dem, så du mere specifikt kan målrette mod tumorer, og rekruttere også andre celler eller molekyler til at angribe tumorcellerne uden mange bivirkninger. Vi tror virkelig, det er vejen frem."
 Varme artikler
Varme artikler
-
 LED-vej:En ren og bekvem metode til at oxidere plastoverflader til industrienFig. 1:Surface oxygenering af sidekædede methylgrupper i polypropylen under fotobestråling med chlordioxid. Kredit:Osaka University Polypropylen (PP) er overalt, er en af de mest anvendte plastm
LED-vej:En ren og bekvem metode til at oxidere plastoverflader til industrienFig. 1:Surface oxygenering af sidekædede methylgrupper i polypropylen under fotobestråling med chlordioxid. Kredit:Osaka University Polypropylen (PP) er overalt, er en af de mest anvendte plastm -
 Hvad sker der, når du tilsætter ammoniumnitrat til vand?Du forbinder måske ammoniumnitrat med sprængstoffer; det er almindeligt anvendt i sikkerhedseksplosiver og pyroteknologi såvel som gødning. Men ikke alle ammoniumnitratforsøg ender med et smell. Nå
Hvad sker der, når du tilsætter ammoniumnitrat til vand?Du forbinder måske ammoniumnitrat med sprængstoffer; det er almindeligt anvendt i sikkerhedseksplosiver og pyroteknologi såvel som gødning. Men ikke alle ammoniumnitratforsøg ender med et smell. Nå -
 En forbedret metode til visualisering af proteinkrystalstrukturEn forbedret metode til visualisering af proteinkrystalstruktur. Kredit:Immanuel Kant Baltic Federal University Teknikken til visualisering af røntgenkrystalstruktur har været kendt i over hundred
En forbedret metode til visualisering af proteinkrystalstrukturEn forbedret metode til visualisering af proteinkrystalstruktur. Kredit:Immanuel Kant Baltic Federal University Teknikken til visualisering af røntgenkrystalstruktur har været kendt i over hundred -
 Video:Hvordan håndsprit virkerKredit:The American Chemical Society Alkoholbaserede håndsprit er de allestedsnærværende små klemflaskehelte i lufthavne og hospitaler, vores allierede i forkølelses- og influenzasæsonen, og angiv
Video:Hvordan håndsprit virkerKredit:The American Chemical Society Alkoholbaserede håndsprit er de allestedsnærværende små klemflaskehelte i lufthavne og hospitaler, vores allierede i forkølelses- og influenzasæsonen, og angiv
- Forskerteam demonstrerer fraktalt lys fra lasere
- Eksponeringen for et nyere flammehæmmer har været stigende
- Mikropartikler skabt ved ny 3D-fremstillingsmetode kunne frigive medicin eller vacciner længe efter…
- Sådan finder du en tangentlinie til en Curve
- Forskere opfinder metode til at frigøre potentialet for meget brugt medicin
- Ting lavet af Tungsten


