Kobber(II)sulfatdehydrering:Forståelse af farveændringen
* Blå farve: Den blå farve af kobber(II)sulfatpentahydrat kommer fra vandmolekylerne, der er koordineret til kobber(II)-ionen (Cu²⁺). Disse vandmolekyler interagerer med kobberionen, påvirker dens elektroniske struktur og giver den en karakteristisk blå farve.
* Opvarmning og dehydrering: Når man opvarmer kobber(II)sulfatpentahydrat, bliver vandmolekylerne drevet af som damp. Denne proces kaldes dehydrering.
* Farveløst vandfrit salt: Når først vandet er fjernet, er kobber(II)-ionen ikke længere omgivet af vandmolekyler. Denne ændring i omgivelserne ændrer dens elektroniske struktur og resulterer i tab af dens blå farve. Det resulterende vandfri kobber(II)sulfat (CuSO4) er et hvidt eller bleggråt fast stof.
Reaktionen kan opsummeres som følger:
CuSO4•5H2O (blå) → CuSO4 (hvid/lysegrå) + 5H2O (g)
Sammenfattende opstår den blå farve af kobber(II)sulfatpentahydrat fra interaktionen mellem kobber(II)ion- og vandmolekylerne. Ved opvarmning fjernes vandmolekylerne, hvilket ændrer kobberionens miljø og får den til at miste sin blå farve.
 Varme artikler
Varme artikler
-
 Juicing teknik kan påvirke sundheden af friskpresset juiceKredit:CC0 Public Domain Med det nye år, mange mennesker tager beslutninger om at spise sundere, ved at spise flere grøntsager, for eksempel. Men dem, der ikke kan lide smagen eller konsistensen a
Juicing teknik kan påvirke sundheden af friskpresset juiceKredit:CC0 Public Domain Med det nye år, mange mennesker tager beslutninger om at spise sundere, ved at spise flere grøntsager, for eksempel. Men dem, der ikke kan lide smagen eller konsistensen a -
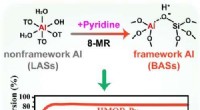 Dynamisk udvikling af aluminiumskoordinationsmiljøer i mordenitzeolitGrafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202210658 Zeolitter er vigtige i mange kemiske syntese og petrokemiske processer. De økonomiske og miljømæs
Dynamisk udvikling af aluminiumskoordinationsmiljøer i mordenitzeolitGrafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202210658 Zeolitter er vigtige i mange kemiske syntese og petrokemiske processer. De økonomiske og miljømæs -
 Efter mere end et årti, ChIP-seq kan trods alt være kvantitativKredit:Unsplash/CC0 Public Domain I mere end et årti, forskere, der studerer epigenetik, har brugt en kraftfuld metode kaldet ChIP-seq til at kortlægge ændringer i proteiner og andre kritiske regu
Efter mere end et årti, ChIP-seq kan trods alt være kvantitativKredit:Unsplash/CC0 Public Domain I mere end et årti, forskere, der studerer epigenetik, har brugt en kraftfuld metode kaldet ChIP-seq til at kortlægge ændringer i proteiner og andre kritiske regu -
 Forklaret varmekapacitet:Hvordan varme påvirker temperaturenAf Kevin Beck Opdateret 30. august 2022 SubstanceP/iStock/GettyImages Varmekapacitet er et begreb i fysik, der beskriver, hvor meget varme der skal tilføres et stof for at hæve dets temperatur med
Forklaret varmekapacitet:Hvordan varme påvirker temperaturenAf Kevin Beck Opdateret 30. august 2022 SubstanceP/iStock/GettyImages Varmekapacitet er et begreb i fysik, der beskriver, hvor meget varme der skal tilføres et stof for at hæve dets temperatur med
- Skjult trussel:Global underjordisk infrastruktur sårbar over for havniveaustigning
- Hvordan virkede den elastiske kollisionseffekt total momentum og kinetik energi i systemet?
- Når du er ude i solskin, føler du dig varm, fordi energi ophidser molekyler af din hud og skaber v…
- Hvad hedder gener, der ikke gennemgår et uafhængigt sortiment?
- Hvorfor er skolebusser gule?
- Nye NASA -billeder afslører snedækkede Mars -klitter


