Empirisk formel:Forstå flere forbindelser med samme forhold
Her er hvorfor:
* Empirisk formel: Den empiriske formel repræsenterer det enkleste hele talforhold mellem atomer i en forbindelse. Det fortæller os ikke det faktiske antal atomer i et molekyle.
* Molekylformel: Molekylformlen viser det faktiske antal atomer af hvert grundstof i et molekyle.
Eksempler:
* Glucose (C6H12O6) og eddikesyre (C2H4O2): Begge har den samme empiriske formel (CH2O), men deres molekylære formler og strukturer er forskellige.
* Ethylen (C2H4) og Butan (C4H10): Begge har den empiriske formel (CH2), men deres molekylære formler og strukturer er forskellige.
Nøglepunkter:
* Kovalente forbindelser kan have forskellige molekylære formler, men deler den samme empiriske formel på grund af forskellige forhold mellem de samme grundstoffer.
* Den empiriske formel alene giver ikke nok information til at bestemme den nøjagtige struktur eller molekylformel for en kovalent forbindelse.
Derfor er det afgørende at overveje den molekylære formel og andre strukturelle oplysninger for at skelne mellem kovalente forbindelser med den samme empiriske formel.
Sidste artikelIsomerer af C4H10:Butan og isobutan forklaret
Næste artikelKobber(II)sulfatdehydrering:Forståelse af farveændringen
 Varme artikler
Varme artikler
-
 Opbygning af en bedre brændselscelle begynder med overfladekemiForskere kiggede dybt ind i en brændselscelles indre funktioner for at få et mere komplet billede af den katalytiske proces. Dette arbejde lover at forbedre design til mere effektive celler. Kredit:Na
Opbygning af en bedre brændselscelle begynder med overfladekemiForskere kiggede dybt ind i en brændselscelles indre funktioner for at få et mere komplet billede af den katalytiske proces. Dette arbejde lover at forbedre design til mere effektive celler. Kredit:Na -
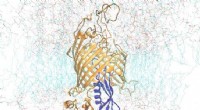 Klik på... Resistente bakterier fanget på fersk gerningMens menneskeheden kæmper mod coronavirus, kampen mod antibiotikaresistente bakterier fortsætter Forskere ved UCLouvain er lykkedes med at fange unikke billeder af proteinsoldater, der hjælper bakteri
Klik på... Resistente bakterier fanget på fersk gerningMens menneskeheden kæmper mod coronavirus, kampen mod antibiotikaresistente bakterier fortsætter Forskere ved UCLouvain er lykkedes med at fange unikke billeder af proteinsoldater, der hjælper bakteri -
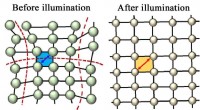 Lys afslapper krystal for at øge solcelleeffektivitetenKonstant belysning blev fundet for at slappe af gitteret af et perovskitlignende materiale, gør det mere effektivt til at opsamle sollys og omdanne det til energi. Det stabile materiale blev testet ti
Lys afslapper krystal for at øge solcelleeffektivitetenKonstant belysning blev fundet for at slappe af gitteret af et perovskitlignende materiale, gør det mere effektivt til at opsamle sollys og omdanne det til energi. Det stabile materiale blev testet ti -
 Forstå tonicitet:osmose og isotoniske løsningerAf John Brennan Opdateret 24. marts 2022 a_Taiga/iStock/GettyImages Når vand på den ene side af en membran indeholder mere opløst stof end vand på den anden side, sker der én af to ting. Hvis det
Forstå tonicitet:osmose og isotoniske løsningerAf John Brennan Opdateret 24. marts 2022 a_Taiga/iStock/GettyImages Når vand på den ene side af en membran indeholder mere opløst stof end vand på den anden side, sker der én af to ting. Hvis det
- Floodplains er en forlængelse af en flod:Hvordan vi forbinder dem, skal ændres
- Genevieve nærmer sig Mexicos Baja som kategori 3-orkan
- Et kig på, hvad NASA's nye rover pakkede til Mars
- Hvad findes et naturligt stof i muskler, der regenererer ATP for udvidet energi?
- Hvilke materialer bruges på solcellepaneler giver dem mulighed for at producere elektricitet?
- Reducer, genbrug, genbrug:Hvordan genetisk modificerede fluer kan reducere affald og holde det væk …


