Aluminiumsfolie og svovlsyrereaktion:kemisk reaktion og forklaring
Reaktion:
* Aluminium (Al) + Svovlsyre (H₂SO₄) → Aluminiumsulfat (Al₂(SO₄)₃) + Hydrogengas (H₂)
Forklaring:
1. Aluminium er mere reaktiv end brint. Det betyder, at det kan fortrænge brint fra sin forbindelse, svovlsyre.
2. Når aluminium kommer i kontakt med svovlsyre, mister det elektroner og danner aluminiumioner (Al³⁺) .
3. Disse aluminiumioner kombineres med sulfationer (SO₄²⁻) fra svovlsyren for at danne aluminiumsulfat (Al₂(SO₄)₃) et opløseligt salt.
4. Samtidig får hydrogenionerne (H⁺) fra svovlsyren elektroner og danner brintgas (H₂) , som frigives som bobler.
Observationer:
* Du vil observere kraftig bobling efterhånden som brintgas frigives.
* Aluminiumsfolien vil opløses gradvist, efterhånden som det reagerer med syren.
* Løsningen bliver varmere på grund af reaktionens eksoterme karakter.
* Hvis koncentrationen af svovlsyren er høj nok, kan opløsningen virke overskyet på grund af dannelsen af aluminiumsulfat.
Vigtig bemærkning:
* Denne reaktion bør udføres med forsigtighed, da den genererer varme og brændbar brintgas. Det er bedst at udføre det under opsyn af en kvalificeret instruktør.
* Reaktionen kan bremses ved at bruge en fortyndet opløsning af svovlsyre eller ved at afkøle reaktionsblandingen.
Samlet set er reaktionen mellem aluminiumsfolie og svovlsyre en klassisk demonstration af metallers reaktivitet og dannelsen af salte og gasser.
 Varme artikler
Varme artikler
-
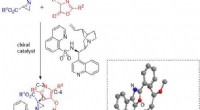 Asymmetrisk syntese af aziridin med en ny katalysator kan hjælpe med at udvikle nye lægemidlerFremstilling af aziridiner med højt udbytte og høj renhed ved hjælp af ny katalysator. Forskere fra Japan foreslog for nylig en mulig overgangstilstand for reaktionen mellem aziridiner og oxazoloner i
Asymmetrisk syntese af aziridin med en ny katalysator kan hjælpe med at udvikle nye lægemidlerFremstilling af aziridiner med højt udbytte og høj renhed ved hjælp af ny katalysator. Forskere fra Japan foreslog for nylig en mulig overgangstilstand for reaktionen mellem aziridiner og oxazoloner i -
 Groovy fotoelektroder:Hvordan en tekstureret overflade dramatisk kan øge ydeevnenUd over store riller, som var til stede før ætsningen, høj tæthed af små riller blev observeret på overfladerne efter ætsning. Kredit:NITech I den nuværende sammenhæng vedrørende CO 2 niveauer o
Groovy fotoelektroder:Hvordan en tekstureret overflade dramatisk kan øge ydeevnenUd over store riller, som var til stede før ætsningen, høj tæthed af små riller blev observeret på overfladerne efter ætsning. Kredit:NITech I den nuværende sammenhæng vedrørende CO 2 niveauer o -
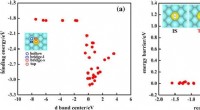 AI ledte efter enkeltatom-legeringskatalysatorer, fundet 200 lovende kandidaterFig. 1:Korrelation mellem simple deskriptorer og målegenskaber. Skoltech-forskere og deres kolleger fra Kina og Tyskland har præsenteret en ny søgealgoritme efter single-atom-legeringskatalysatore
AI ledte efter enkeltatom-legeringskatalysatorer, fundet 200 lovende kandidaterFig. 1:Korrelation mellem simple deskriptorer og målegenskaber. Skoltech-forskere og deres kolleger fra Kina og Tyskland har præsenteret en ny søgealgoritme efter single-atom-legeringskatalysatore -
 Stiller ind på morgendagens LCD-skærme:Udforsk den nye IGZO-11-halvlederKredit:CC0 Public Domain I 1985, Noboru Kimizuka fra det nationale institut for forskning i uorganiske materialer, Japan havde banebrydende ideen om polykrystallinsk indium-gallium-zinkoxid (IGZO)
Stiller ind på morgendagens LCD-skærme:Udforsk den nye IGZO-11-halvlederKredit:CC0 Public Domain I 1985, Noboru Kimizuka fra det nationale institut for forskning i uorganiske materialer, Japan havde banebrydende ideen om polykrystallinsk indium-gallium-zinkoxid (IGZO)
- Hvorfor er kroppen vægtløs i rummet?
- Ny finansiering til forskning i supermateriale grafen
- Hvordan producerer planter mad fra energien?
- Der kan være op til 70 gange mere brint i Jordens kerne end i havene
- Hvad ville der ske, hvis Jorden pludselig holdt op med at rotere? De virkelige videnskabelige konsek…
- Videospilsindsats kan hjælpe med at regulere fremtidig dronetrafik


