Tribromid (Br₃⁻) Molekylær geometri:Forstå bindingsvinkler og -form
* Bor's Hybridization: Bor i tribromid har sp² hybridisering. Det betyder, at den danner tre sigma-bindinger ved at bruge en 2s og to 2p orbitaler.
* Ensomme par: Det centrale boratom har ingen enlige elektronpar.
* VSEPR-teori: Ifølge Valence Shell Electron Pair Repulsion (VSEPR) teorien vil elektronparrene omkring det centrale atom arrangere sig selv for at minimere frastødningen. I dette tilfælde vil de tre bindingspar (fra bromatomerne) arrangere sig så langt fra hinanden som muligt, hvilket resulterer i en lineær geometri.
Derfor er den molekylære geometri af tribromid (Br₃⁻) lineær.
 Varme artikler
Varme artikler
-
 Et enkelt enzym inducerer det kemiske forsvar af en svamp mod larverKredit:Wiley Nogle svampe producerer langkædede umættede carboxylsyrer som deres kemiske forsvar mod insektlarver. Biosyntesen af disse polyener er kun afhængig af ét enzym, som tyske videnskabs
Et enkelt enzym inducerer det kemiske forsvar af en svamp mod larverKredit:Wiley Nogle svampe producerer langkædede umættede carboxylsyrer som deres kemiske forsvar mod insektlarver. Biosyntesen af disse polyener er kun afhængig af ét enzym, som tyske videnskabs -
 Elektrisk ledende maling og andre polymerlegeringer fremstilles nu letForskere fra University of Tsukuba og samarbejdspartnere fremstillede polyanilin i en lang række billige opløsningsmidler. Denne udvikling vil lette avancerede anvendelser inden for printkort og andre
Elektrisk ledende maling og andre polymerlegeringer fremstilles nu letForskere fra University of Tsukuba og samarbejdspartnere fremstillede polyanilin i en lang række billige opløsningsmidler. Denne udvikling vil lette avancerede anvendelser inden for printkort og andre -
 Glykaner som biomarkører for kræft?Kredit:Wiley Glykosylerede proteiner er ofte overudtrykt i tumorceller og kan derfor tjene som tumormarkører, især dem med det interessante molekyle sialinsyre som sukkerdel. I journalen Angewand
Glykaner som biomarkører for kræft?Kredit:Wiley Glykosylerede proteiner er ofte overudtrykt i tumorceller og kan derfor tjene som tumormarkører, især dem med det interessante molekyle sialinsyre som sukkerdel. I journalen Angewand -
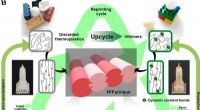 Upcycling af plast gennem dynamisk tværbindingCirkulær modeldesign af upcycling af termoplast til genanvendelig vitrimer til FFF. (A) Skematisk diagram, der sammenligner karakteristika for traditionelle termoplast, termohærdende og vitrimere. (B)
Upcycling af plast gennem dynamisk tværbindingCirkulær modeldesign af upcycling af termoplast til genanvendelig vitrimer til FFF. (A) Skematisk diagram, der sammenligner karakteristika for traditionelle termoplast, termohærdende og vitrimere. (B)
- Dens krystaller sublime som violet gasiod eller brom?
- Matematikere beviser, at flash-hukommelse fingeraftryk af elektroniske enheder er virkelig unikke
- Hvilken type elementer er metaller Rhodium Platinum og Palladium?
- Hvad kan differentiere gennem hele livet i den menneskelige krop?
- Hvad er det sammensatte navn på lithium svovl?
- Sådan identificeres en edderkop af Web Pattern


