Reaktivitet af ikke-metaller:tendenser og forklaringer
* Elektronegativitet: Ikke-metaller har en højere elektronegativitet end metaller. Det betyder, at de har en stærkere tiltrækning af elektroner. Når du bevæger dig hen over en periode, øges elektronegativiteten. Dette gør ikke-metaller mere tilbøjelige til at få elektroner og danne negative ioner, hvilket fører til større reaktivitet.
* Ioniseringsenergi: Ioniseringsenergi er den energi, der kræves for at fjerne en elektron fra et atom. Når du bevæger dig hen over en periode, øges ioniseringsenergien. Dette betyder, at det bliver sværere at fjerne elektroner fra ikke-metalatomerne, hvilket gør dem mindre tilbøjelige til at miste elektroner og mere tilbøjelige til at få dem, hvilket yderligere forbedrer reaktiviteten.
* Atomstørrelse: Atomstørrelse falder, når du bevæger dig hen over en periode. Dette betyder, at de ydre elektroner er tættere på kernen og oplever en stærkere tiltrækning. Dette bidrager igen til ikke-metallets tendens til at få elektroner, hvilket fører til større reaktivitet.
Eksempler:
* Gruppe 17 (halogener): Fluor (F) er det mest reaktive ikke-metal i denne gruppe, efterfulgt af klor (Cl), brom (Br), jod (I) og astatin (At). Denne tendens observeres, fordi fluor har den højeste elektronegativitet og mindste atomstørrelse inden for gruppen.
* Gruppe 16 (Chalcogener): Ilt (O) er mere reaktivt end svovl (S), som er mere reaktivt end selen (Se).
Undtagelser:
Mens den generelle tendens er en stigning i reaktivitet over en periode for ikke-metaller, er der undtagelser. For eksempel er ædelgasserne (Gruppe 18) generelt ikke-reaktive på grund af deres fulde ydre elektronskaller.
 Varme artikler
Varme artikler
-
 Bifile overflader reducerer afrimningstider i varmevekslereTime-lapse billeder af dynamisk afrimning på superhydrofobe og bifile overflader. Tidspunktet t =0 repræsenterer det tidspunkt, hvor smeltning af frost først blev observeret visuelt. Kredit:Nenad Milj
Bifile overflader reducerer afrimningstider i varmevekslereTime-lapse billeder af dynamisk afrimning på superhydrofobe og bifile overflader. Tidspunktet t =0 repræsenterer det tidspunkt, hvor smeltning af frost først blev observeret visuelt. Kredit:Nenad Milj -
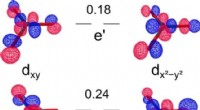 Forsker opdager ny oxidationstilstand for rhodiumGrænse naturlig molekylær orbital plot ved 0,1 e Bohr−3 (statsspecifik CASSCF(15,20)/aug-cc-pVTZ-DK) for 1 A1 elektronisk grundtilstand i D3h punktgruppesymmetri af [RhO3 ]+ . Kredit:Angewandte Chemi
Forsker opdager ny oxidationstilstand for rhodiumGrænse naturlig molekylær orbital plot ved 0,1 e Bohr−3 (statsspecifik CASSCF(15,20)/aug-cc-pVTZ-DK) for 1 A1 elektronisk grundtilstand i D3h punktgruppesymmetri af [RhO3 ]+ . Kredit:Angewandte Chemi -
 At lære nye tricks fra havsvampe, naturens mest usandsynlige civilingeniørerGlasfibrene, der udgør Euplectella aspergillum-svampen, er overraskende stærke og fleksible. Kredit:Michael A Monn, CC BY-ND Forestil dig en fremtid, hvor bygninger knejser kilometervis over gader
At lære nye tricks fra havsvampe, naturens mest usandsynlige civilingeniørerGlasfibrene, der udgør Euplectella aspergillum-svampen, er overraskende stærke og fleksible. Kredit:Michael A Monn, CC BY-ND Forestil dig en fremtid, hvor bygninger knejser kilometervis over gader -
 Det bedste fra begge verdener:Høj entropi møder lave dimensioner, åbner op for uendelige mulighed…Kredit:Tokyo Tech Opdagelsen af grafen, en 2D lagdelt form af kulstof, engang forårsagede et paradigmeskifte inden for videnskab og teknologi som ingen anden. Da dette vidundermateriale tiltrak
Det bedste fra begge verdener:Høj entropi møder lave dimensioner, åbner op for uendelige mulighed…Kredit:Tokyo Tech Opdagelsen af grafen, en 2D lagdelt form af kulstof, engang forårsagede et paradigmeskifte inden for videnskab og teknologi som ingen anden. Da dette vidundermateriale tiltrak
- Virksomheder bruger offentlige tilskud til at lette gældsbyrden
- Online nekrologer ændrer den måde, vi offentligt husker døde på, og hvordan aviser dækker døds…
- Hvordan løser du 15-X kuber?
- Tusindvis af børn har ikke set forældre i et år:Skjult indvirkning af COVID på fangerfamilier
- Når natrium og klor kombineres kemisk, hvilket navn gives til det dannede stof?
- Kosmisk daggry rummer svarene på mange af astronomiens største spørgsmål


