Forståelse af aktiveringsenergi i endergoniske reaktioner
Af Brooke Yool, Opdateret 30. august 2022
Reaktionsenergi
I kemi omtaler vi reaktionsbeholderen som "systemet" og alt andet som "omgivelserne". En endergonisk reaktion trækker energi fra omgivelserne ind i systemet, mens en eksergonisk reaktion frigiver energi fra systemet til omgivelserne.
Alle reaktioner kræver et første input af energi - aktiveringsenergien - for at begynde. For eksempel frigiver træforbrænding varme, når den starter, men den har stadig brug for en flamme for at antænde og levere den oprindelige energi.
Aktiveringsenergi
For at gå fra reaktanter til produkter skal en reaktion overvinde sin unikke aktiveringsenergibarriere. Barrierens højde er uafhængig af om reaktionen er endergonisk eller eksergonisk; en meget eksergonisk reaktion kan stadig have en væsentlig barriere, og omvendt.
Mange reaktioner forløber gennem flere trin, hver med sin egen aktiveringsenergitærskel.
Eksempler
Endergoniske processer bygger typisk større strukturer. Proteinsyntese og fotosyntetisk glukosedannelse absorberer begge energi. De omvendte reaktioner – cellulær respiration af glucose og nedbrydning af proteiner – er eksergoniske og frigiver energi.
Katalysatorer
Katalysatorer sænker aktiveringsenergien ved at stabilisere overgangstilstande, hvilket effektivt skaber en lavere energivej for reaktionen. Enzymer, de mest almindelige biologiske katalysatorer, er eksempler på dette princip.
Reaktionsspontanitet
Kun eksergoniske reaktioner opstår spontant, fordi de frigiver energi. Endergoniske processer, såsom muskelopbygning eller DNA-replikation, drives af kobling med eksergoniske reaktioner, der leverer den nødvendige energiforskel.
 Varme artikler
Varme artikler
-
 Trin-for-trin guide til garvning af fårehuder derhjemmeaf Scarlett Gauthier Opdateret 24. marts 2022 Mange vælger at garve fårehuder for at bevare alle dele af dyret og skabe smukke tæpper eller dekorative stykker. Selvom professionel garvning er almind
Trin-for-trin guide til garvning af fårehuder derhjemmeaf Scarlett Gauthier Opdateret 24. marts 2022 Mange vælger at garve fårehuder for at bevare alle dele af dyret og skabe smukke tæpper eller dekorative stykker. Selvom professionel garvning er almind -
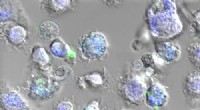 En ny slags vaccine baseret på edderkoppesilkeImmunceller, der indtog nanopartikler af edderkoppesilke (i grønt). Endosomerne - den del af cellen, hvori nanopartiklerne frigiver vaccinen - vises i blåt. Kredit:Laboratoire Bourquin – UNIGE For
En ny slags vaccine baseret på edderkoppesilkeImmunceller, der indtog nanopartikler af edderkoppesilke (i grønt). Endosomerne - den del af cellen, hvori nanopartiklerne frigiver vaccinen - vises i blåt. Kredit:Laboratoire Bourquin – UNIGE For -
 Nøglen til kulfrie biler? Se til stjernerneIllustration af en supernovaeksplosion. Sådanne hvirvlende masser af stof gav form til de tidligste former for kulstof - forstadier til molekyler, som nogle forskere siger, er forbundet med syntesen a
Nøglen til kulfrie biler? Se til stjernerneIllustration af en supernovaeksplosion. Sådanne hvirvlende masser af stof gav form til de tidligste former for kulstof - forstadier til molekyler, som nogle forskere siger, er forbundet med syntesen a -
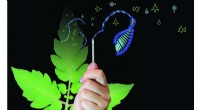 Dipstick-teknologi kan revolutionere sygdomsdiagnostikMålepinden kan rense DNA og RNA fra planter, dyre- og mikrobeprøver på mindre end 30 sekunder. Kredit:Michael Mason Ny målepindsteknologi, der muliggør patogendetektion og hurtig diagnosticering a
Dipstick-teknologi kan revolutionere sygdomsdiagnostikMålepinden kan rense DNA og RNA fra planter, dyre- og mikrobeprøver på mindre end 30 sekunder. Kredit:Michael Mason Ny målepindsteknologi, der muliggør patogendetektion og hurtig diagnosticering a


