Hvorfor enzymer fejler:Varmeinduceret denaturering og kemisk hæmning
Creatas/Creatas/Getty Images
Enzymer er specialiserede proteiner, der katalyserer biokemiske reaktioner ved at vedtage præcise tredimensionelle strukturer. Når deres form er forstyrret, mister de aktivitet. To primære mekanismer reducerer enzymeffektiviteten:varmeinduceret denaturering og kemisk hæmning.
Denaturering ved varme
I et stabilt enzym vibrerer atomer, men proteinkæden forbliver foldet. At hæve temperaturen øger molekylær bevægelse, hvilket i sidste ende får enzymet til at udfolde sig og miste sin funktionelle konformation. De fleste dyreenzymer når topaktivitet nær fysiologisk temperatur (≈37°C) og begynder at miste aktivitet, når temperaturen overstiger omkring 40°C. Ekstremofile bakterier har imidlertid enzymer, der kan modstå temperaturer tæt på kogepunktet, hvilket gør dem i stand til at trives i varme kilder.
Aktivt websted:The Reaction Hub
Det aktive sted er enzymets katalytiske lomme, analogt med en mund, der holder substratet. Korrekt justering af specifikke aminosyresidekæder er afgørende for at binde substratet og lette den kemiske transformation. Hvis det aktive steds 3D-form er forvrænget, kan enzymet ikke udføre sin reaktion.
Konkurrencehæmmere
Konkurrerende inhibitorer efterligner substratet og binder sig direkte til det aktive sted, hvilket blokerer substratadgang. Fordi de kan dissociere, er mange reversible og tillader enzymet at genvinde aktivitet, når inhibitoren er fjernet.
Ikke-konkurrencedygtige (allosteriske) hæmmere
Disse inhibitorer binder sig til andre regulatoriske steder end det aktive sted. Binding ændrer enzymets konformation, hvilket effektivt lukker eller deaktiverer det aktive sted. Allosterisk hæmning kan samtidig dæmpe hele enzymkomplekser, når en enkelt hæmmer binder til en underenheds regulatoriske region.
Forståelse af disse mekanismer er afgørende for områder lige fra lægemiddeldesign til industriel bioteknologi.
 Varme artikler
Varme artikler
-
 Producerer billigere, grønnere hydrogenperoxidKredit:Pixabay/CC0 Public Domain Australske forskere under ledelse af University of New South Wales har brugt Australian Synchrotron til at forstå, hvordan den kemiske struktur af et avanceret kat
Producerer billigere, grønnere hydrogenperoxidKredit:Pixabay/CC0 Public Domain Australske forskere under ledelse af University of New South Wales har brugt Australian Synchrotron til at forstå, hvordan den kemiske struktur af et avanceret kat -
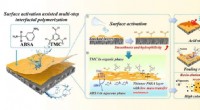 Nye syrefaste membraner til spildevandsrensning udvikletSkematisk mekanisme til fremstilling af syrefast nanofiltreringsmembran og dens overlegne separationsydelse. Kredit:CAO Yang En forskergruppe ledet af prof. Wan Yinhua fra Institute of Process Eng
Nye syrefaste membraner til spildevandsrensning udvikletSkematisk mekanisme til fremstilling af syrefast nanofiltreringsmembran og dens overlegne separationsydelse. Kredit:CAO Yang En forskergruppe ledet af prof. Wan Yinhua fra Institute of Process Eng -
 Nuklear engineering forskere udvikler ny elastisk oxiddispersion styrket legeringKredit:Pixabay/CC0 Public Domain Forskere fra Texas A&M University har for nylig vist overlegen ydeevne af en ny oxiddispersion-forstærket (ODS) legering, de udviklede til brug i både fissions- og
Nuklear engineering forskere udvikler ny elastisk oxiddispersion styrket legeringKredit:Pixabay/CC0 Public Domain Forskere fra Texas A&M University har for nylig vist overlegen ydeevne af en ny oxiddispersion-forstærket (ODS) legering, de udviklede til brug i både fissions- og -
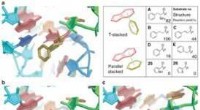 Hærprojekt kan føre til en ny klasse af højtydende materialerSyntetiske biologer, der arbejder på et amerikansk hærsprojekt, har udviklet et sæt designregler, der guider hvordan ribosomer, en cellestruktur, der danner protein, kunne føre til en ny klasse af syn
Hærprojekt kan føre til en ny klasse af højtydende materialerSyntetiske biologer, der arbejder på et amerikansk hærsprojekt, har udviklet et sæt designregler, der guider hvordan ribosomer, en cellestruktur, der danner protein, kunne føre til en ny klasse af syn
- Hvad er de tre kirtler af et reproduktionssystem for mænd?
- Tre kvinder er forstanden bag Google Assistants personlighed
- Hvad er de forskellige typer udtryk, som folk bruger?
- Forståelse af kondensering:Hvordan vanddamp bliver flydende
- Xiaomi:En kinesisk opstart for at udfordre Google, Amazon
- Hvorfor absorberer en mørk farve mere varme end hvid farve?


