Konverter normalitet til gram:Trin-for-trin guide til nøjagtige beregninger
Af bidragende skribent – Opdateret 30. august 2022
Pattanaphong Khuankaew/iStock/GettyImages
En opløsnings koncentration beskriver, hvor meget opløst stof der er opløst pr. volumenhed. Mens molaritet (molL⁻¹) tæller mol, tæller normalitet (N) kemiske ækvivalenter - i det væsentlige antallet af reaktive enheder et opløst stof kan give. For eksempel donerer svovlsyre (H₂SO4) to protoner, så en 1M H₂SO4-opløsning har en normalitet på 2N.
Nedenfor er en kortfattet, trin-for-trin metode til at konvertere en normalitetsværdi til massen af opløst stof i gram. Vi bruger 240mL af en 2,5N H₂SO₄-opløsning som et kørende eksempel.
1. Saml atomvægte
Se en pålidelig periodisk tabel for at finde atommasserne:H=1,01gmol⁻¹, S=32,07gmol⁻¹, O=16,00gmol⁻¹.
2. Beregn molmassen
Tilføj vægten af alle atomer i formlen:(2×1,01)+32,07+(4×16,00)=98,09gmol⁻¹.
3. Bestem den ækvivalente masse
Divider den molære masse med antallet af protoner frigivet ved dissociation. For H2SO4 er reaktionen H2SO4→2H++SO4²⁻, så den ækvivalente masse er 98,09/2=49,05gequiv⁻1.
4. Konverter volumen til liter
240mL svarer til 0,240L.
5. Beregn massen af opløst stof
Multiplicer normalitet, ækvivalent masse og volumen:2,5N×49,05gequiv⁻¹×0,240L=29,34g (≈29,4g).
Værktøjer, du skal bruge
- Ajourført periodisk system
- Videnskabelig lommeregner eller regneark
Følg denne rutine for enhver normalitet-til-gram-konvertering, og du vil opnå præcise, reproducerbare resultater - afgørende for både laboratoriearbejde, industrielle processer og uddannelseslaboratorier.
Sidste artikelSådan tælles atomer nøjagtigt i kemiske formler
Næste artikelUnderstanding CO₂ Density:From Gases to Dry Ice
 Varme artikler
Varme artikler
-
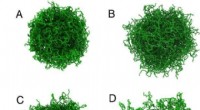 Tætte mikrogelsuspensioner afslører in-silico, hvad der sker under kompressionSimuleringssnapshots af hævede mikrogelpartikler. (Top) Mikrogeler, der har en ensartet tværbindingsfordeling, og (bund) mikrogeler, der har en Gaussisk tværbindingsfordeling. Kredit:Georgia Tech
Tætte mikrogelsuspensioner afslører in-silico, hvad der sker under kompressionSimuleringssnapshots af hævede mikrogelpartikler. (Top) Mikrogeler, der har en ensartet tværbindingsfordeling, og (bund) mikrogeler, der har en Gaussisk tværbindingsfordeling. Kredit:Georgia Tech -
 Blandeløsninger i verdens mindste reagensglasKredit:University of Manchester Forskere baseret på University of Manchester har demonstreret en ny metode til billeddannelse af levende kemiske reaktioner med atomopløsning ved hjælp af reagensgl
Blandeløsninger i verdens mindste reagensglasKredit:University of Manchester Forskere baseret på University of Manchester har demonstreret en ny metode til billeddannelse af levende kemiske reaktioner med atomopløsning ved hjælp af reagensgl -
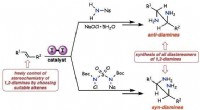 Molekylært jod katalyserer processer til antivirale og farmaceutiske synteserFigur 1. Skematisk diagram af anti- og syn-diamineringerne af alkener ved anvendelse af jodkatalysator. Kredit:Osaka University Syntetisering af lægemidler til kræft, virale sygdomme, og andre med
Molekylært jod katalyserer processer til antivirale og farmaceutiske synteserFigur 1. Skematisk diagram af anti- og syn-diamineringerne af alkener ved anvendelse af jodkatalysator. Kredit:Osaka University Syntetisering af lægemidler til kræft, virale sygdomme, og andre med -
 Redesigner håndsprit og donerer 7, 000 gallons til at bekæmpe COVID-19Håndsprit reddet af ethanol. Et velgørende initiativ kørte for at forhindre håndsprit i at løbe kritisk lavt over hele landet. Kredit:Georgia Tech/Christopher Moore Så mange mennesker, Seth Marder
Redesigner håndsprit og donerer 7, 000 gallons til at bekæmpe COVID-19Håndsprit reddet af ethanol. Et velgørende initiativ kørte for at forhindre håndsprit i at løbe kritisk lavt over hele landet. Kredit:Georgia Tech/Christopher Moore Så mange mennesker, Seth Marder
- Hvor mange newton droppede 1 kg fra meterprodukter?
- Hollandske astronomer opdager opskriften på at lave kosmisk glycerol
- Hvad betyder Elecitral Energy?
- Revolveres Sun om ethvert himmelsk legeme?
- Den menneskelige krop begynder typisk at blive koloniseret af sin normale flora, hvornår?
- Grundstofferne cæsium Barium og lutetium optræder fra venstre mod højre i periode 6 af det period…


