Konvertering af joule til muldvarpe:En praktisk guide
Af Alan Sembera – Opdateret 30. august 2022
Når man studerer energetikken i en kemisk reaktion, er det ofte nødvendigt at bestemme, hvor mange mol af en reaktant, der var involveret, baseret på energiændringen målt i joule. Fordi en joule kvantificerer energi, og en mol kvantificerer mængden af stof, kræver konvertering mellem de to kendskab til reaktionens entalpiændring pr. mol (ΔHJmol⁻¹).
Trin 1 – Identificer reaktionens standardentalpiændring
For hver specifik reaktion er mængden af frigivet eller absorberet energi pr. mol stof en fast værdi. For eksempel er opløsningen af natriumhydroxid i vand eksoterm og frigiver ca. 55200 J pr. mol NaOH.
Trin 2 – Mål den samlede energiændring
Brug kalorimetriske data eller andre pålidelige metoder til at bestemme den samlede joule frigivet eller absorberet under reaktionen.
Trin 3 – Konverter joule til mol
Divider den målte energi (i joule) med reaktionens entalpiændring pr. mol. Hvis der blev frigivet 30000J, er beregningen 30000J ÷ 55200Jmol⁻¹ ≈ 0,54mol NaOH.
 Varme artikler
Varme artikler
-
 Nyt isoleringsmateriale giver en mere effektiv eldistributionKredit:Chalmers Tekniske Universitet Højspændings jævnstrømskabler, som effektivt kan transportere elektricitet over lange afstande, spiller en afgørende rolle i vores elforsyning. At optimere der
Nyt isoleringsmateriale giver en mere effektiv eldistributionKredit:Chalmers Tekniske Universitet Højspændings jævnstrømskabler, som effektivt kan transportere elektricitet over lange afstande, spiller en afgørende rolle i vores elforsyning. At optimere der -
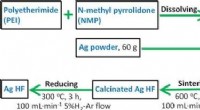 Forskere foreslår en ny metode til at forbedre den elektrokatalytiske omdannelse af kuldioxidDiagram over de detaljerede fremstillingsprocedurer for Ag HF. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202210432 Et forskerhold ledet af Profs. Chen Wei og Wei Wei f
Forskere foreslår en ny metode til at forbedre den elektrokatalytiske omdannelse af kuldioxidDiagram over de detaljerede fremstillingsprocedurer for Ag HF. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202210432 Et forskerhold ledet af Profs. Chen Wei og Wei Wei f -
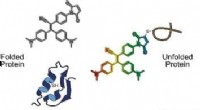 Molekylær sondekort forkert foldet proteometilstand i levende cellerKredit:Wiley Proteinernes foldningstilstand i levende celler afspejler ofte cellens generelle helbred. Australske forskere har udviklet en molekylær sonde, der registrerer proteometilstanden - hel
Molekylær sondekort forkert foldet proteometilstand i levende cellerKredit:Wiley Proteinernes foldningstilstand i levende celler afspejler ofte cellens generelle helbred. Australske forskere har udviklet en molekylær sonde, der registrerer proteometilstanden - hel -
 Forståelse af vandbehandlingsprocessen:Fra spildevand til sikker genbrugPrasit foto/Moment/GettyImages Forbehandling Under forbehandlingen filtreres let aftagelige faste stoffer – såsom grus, olier, fedtstoffer, fedtstoffer og store snavs – ud af den indkommende strøm. P
Forståelse af vandbehandlingsprocessen:Fra spildevand til sikker genbrugPrasit foto/Moment/GettyImages Forbehandling Under forbehandlingen filtreres let aftagelige faste stoffer – såsom grus, olier, fedtstoffer, fedtstoffer og store snavs – ud af den indkommende strøm. P
- En amplitude er 0,5 meter, hvis den øges til 1 meter, hvor meget ændrer energi?
- Hvad er strimler af vekslende magnetiske polariteter, der findes i klipper havbassinerne?
- Tomater af samme kvalitet som normalt, men bruger kun halvdelen af vandet
- Hvad er kilden, der opretholder en konstant værdi af potentiel energi i sin terminal?
- Formede solen før planeter?
- Maskinindlæringsmodel forudsiger fænomenets nøgle til forståelse af materielle egenskaber


