Når brint møder ilt:Den kraftige eksoterme reaktion, der danner vand
Af Clare Jackson | Opdateret 30. august 2022
Zolnierek/iStock/GettyImages
TL;DR
Brint og ilt kombineres eksplosivt og danner vand og frigiver en betydelig mængde varme.
Brint og iltblanding
Ved omgivelsestemperatur eksisterer hydrogen (H₂) og oxygen (O₂) gasser uden at reagere, fordi deres molekyler mangler tilstrækkelig kinetisk energi til at bryde eksisterende bindinger under kollisioner. Blandingen er stabil, indtil en ekstern energikilde starter reaktionen.
Aktiveringsenergi
Indførelse af en gnist eller varme hæver temperaturen på nogle molekyler, hvilket øger deres kollisionsenergi. Når energien overstiger den beskedne aktiveringstærskel for brint (ca. 0,3eV pr. binding), danner H₂- og O₂-molekylerne nye kovalente bindinger, der producerer vand.
Eksoterm reaktion
Brint og ilt har højere indre energi end de resulterende vandmolekyler. Følgelig frigiver reaktionen energi som varme, lys og lyd. Den eksoterme natur driver en kædereaktion, der hurtigt udbreder forbrændingen gennem den resterende blanding.
Elektronadfærd
På et elektronisk niveau deler brintatomer deres enkelte elektroner for at fylde den indre skal af to elektroner, mens oxygenatomer deler fire elektroner for at fuldende deres ydre skal på otte. Det mest stabile arrangement opnås, når to hydrogenatomer hver deler en elektron med et enkelt oxygenatom, der danner H2O-molekylet. Denne omlægning frigiver den energiforskel, der fremmer reaktionen.
Produkter
De primære produkter er vand (H2O) og varme. Den frigivne varme kan udnyttes til arbejde – såsom at drive turbiner – selvom reaktionen i det væsentlige er irreversibel under normale forhold.
 Varme artikler
Varme artikler
-
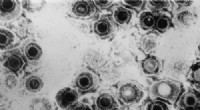 Kryo-elektronmikroskopi afslører almindelig herpesvirusstrukturHerpes simplex virus. Kredit:CDC For første gang, forskere har været i stand til at bruge kryo-elektronmikroskopi, at afsløre den detaljerede struktur af den almindelige herpesvirus. Forskere ved
Kryo-elektronmikroskopi afslører almindelig herpesvirusstrukturHerpes simplex virus. Kredit:CDC For første gang, forskere har været i stand til at bruge kryo-elektronmikroskopi, at afsløre den detaljerede struktur af den almindelige herpesvirus. Forskere ved -
 Afslører strukturen af den mystiske blå hvirvlende flammeEt team af forskere, der arbejder ved University of Maryland, har afdækket strukturen af den mystiske blå hvirvlende flamme. I deres papir offentliggjort i tidsskriftet Videnskab fremskridt , grup
Afslører strukturen af den mystiske blå hvirvlende flammeEt team af forskere, der arbejder ved University of Maryland, har afdækket strukturen af den mystiske blå hvirvlende flamme. I deres papir offentliggjort i tidsskriftet Videnskab fremskridt , grup -
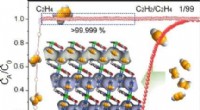 Adskillelse af sporacetylen fra ethylen i ultramikroporøse metal-organiske rammerKredit:Angewandte Chemie Ethylen, en vigtig råvare i den kemiske industri, indeholder ofte spor af acetylenforureninger, som skal fjernes. I journalen Angewandte Chemie , forskere beskriver en r
Adskillelse af sporacetylen fra ethylen i ultramikroporøse metal-organiske rammerKredit:Angewandte Chemie Ethylen, en vigtig råvare i den kemiske industri, indeholder ofte spor af acetylenforureninger, som skal fjernes. I journalen Angewandte Chemie , forskere beskriver en r -
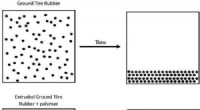 Polymerer baner vejen for bredere brug af genbrugsdæk i asfaltKredit:American Chemical Society Hvert år, omkring 27 millioner dæk ender på lossepladser, lossepladser og lagre, hvor de udgør en sundheds- og miljøfare. Disse dæk kunne få et nyt liv som kompone
Polymerer baner vejen for bredere brug af genbrugsdæk i asfaltKredit:American Chemical Society Hvert år, omkring 27 millioner dæk ender på lossepladser, lossepladser og lagre, hvor de udgør en sundheds- og miljøfare. Disse dæk kunne få et nyt liv som kompone
- Ville en kulstofafgift hjælpe med at innovere mere effektivt energiforbrug?
- Grafen-baserede optiske modulatorer klar til at bryde hastighedsgrænser i digital kommunikation
- .25 g zink reagerede med 10 ml HCI, hvad er molerne reageret?
- Hvad er forskellen mellem jernsulfat og Ferrex 150?
- Pærer celler og switches er alle kredsløb hvad?
- Hvad er dele af de enkle kredsløb?


