Fem praktiske salteksempler til kemi-laboratorier
Af David Weedmark – Opdateret 30. august 2022
At forstå salte er afgørende for ethvert kemipensum. Et salt er en ionisk forbindelse dannet ved neutralisering af en syre og en base, som dissocieres til ioner i vand. Afhængig af den relative styrke af ionerne, kan den resulterende vandige opløsning være sur, basisk eller neutral.
TL;DR
Saltnavne følger konventionen om at angive kationen først, efterfulgt af anionen. For eksempel er bordsalt natriumchlorid (NaCl).
Natriumchlorid (NaCl)
Almindeligvis kendt som bordsalt, natriumchlorid er det hyppigst forekommende salt i både laboratorie- og kulinariske omgivelser. I sin faste tilstand danner NaCl et kubisk gitter og er sikkert at håndtere. Na⁺-ionen er en meget svag Lewis-syre på grund af dens store ionradius og lave ladningstæthed, mens Cl⁻-ionen i det væsentlige opfører sig som en neutral base. Når NaCl er opløst i vand, producerer det en neutral opløsning, hvilket gør det til et standard referencesalt i mange analytiske protokoller.
Kaliumdichromat (K₂Cr₂O₇)
Kaliumdichromat er et orangefarvet oxiderende salt, der indeholder kalium, krom og oxygen. Det er meget giftigt og et kendt kræftfremkaldende stof, især på grund af dets kromatindhold. Laboratorier skal behandle det med forsigtighed:Bær nitrilhandsker, arbejd under et stinkskab, og neutraliser spild med en fortyndet natriumbicarbonatopløsning før bortskaffelse. På grund af dets oxiderende egenskaber udgør det en brandrisiko og bør aldrig kasseres sammen med almindeligt affald.
Calciumchlorid (CaCl₂)
Calciumchlorid deler et hvidt udseende med NaCl, men giver en overlegen afisningsydelse. Det dissocierer i tre ioner (Ca²⁺ og 2 Cl⁻) sammenlignet med NaCls to, hvilket tillader det at smelte is ned til –25°F (–39°C). Dens hygroskopiske natur betyder, at den let absorberer atmosfærisk fugt og danner en flydende opløsning, selv når den efterlades utildækket. Denne egenskab gør den værdifuld til vejbehandling og til laboratorietørringsmidler.
Natriumbisulfat (NaHSO₄)
Afledt af svovlsyre bevarer natriumbisulfat en sur proton, hvilket giver den sure egenskaber. Det er meget brugt som en tør syre i kommercielle applikationer såsom pH-justering til spabade, poolvedligeholdelse og betonrensning. Det faste salt fremstår som hvide perler. Det er farligt for hud og indtagelse; derfor anbefales nitrilhandsker, og øjeblikkelig lægehjælp bør søges ved indtagelse.
Kobbersulfat (CuSO₄)
Kobbersulfat er et blåt krystallinsk salt sammensat af kobber, svovl og oxygen. Ved opløsning bliver opløsningen farveløs. Når en jerngenstand kommer i kontakt med CuSO4, aflejres en rød film af metallisk kobber på jernoverfladen - et klassisk eksempel på en forskydningsreaktion, hvor jern erstatter kobber i opløsning for at danne jern(II)sulfat. Dette fænomen demonstreres ofte i klasseværelsesdemonstrationer af redoxkemi.
 Varme artikler
Varme artikler
-
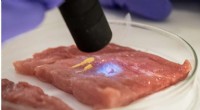 Forskere udvikler biogummilim til hurtigere kirurgisk bedring og smertelindringFlydende CaproGlu påført kød, der er hærdet med UV-lys, bliver til biogummi. Kredit:Nanyang Technological University Materialeforskere fra Nanyang Technological University, Singapore (NTU Singapor
Forskere udvikler biogummilim til hurtigere kirurgisk bedring og smertelindringFlydende CaproGlu påført kød, der er hærdet med UV-lys, bliver til biogummi. Kredit:Nanyang Technological University Materialeforskere fra Nanyang Technological University, Singapore (NTU Singapor -
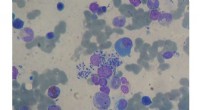 Shagene En syntese perfektioneret til behandling af leishmaniasisKnoglemarvsaspiration:Leishmaniasis (Leishmania sp.) Hos levertransplanteret modtager. Kredit:Paulo Henrique Orlandi Mourao, CC BY-SA 3.0 Lige nord for Antarktis og lidt øst for sydspidsen af Sy
Shagene En syntese perfektioneret til behandling af leishmaniasisKnoglemarvsaspiration:Leishmaniasis (Leishmania sp.) Hos levertransplanteret modtager. Kredit:Paulo Henrique Orlandi Mourao, CC BY-SA 3.0 Lige nord for Antarktis og lidt øst for sydspidsen af Sy -
 Spider dragline silke som torsionsaktuator drevet af fugt til applikationer som kunstig muskelI undersøgelsen, Liu et al. brugte dragline silke fra den afbildede edderkoppeart Nephila eduli, Nephila pilipes og Argiope versicolor. Billedkredit:Spider ID (spiderid.com/pictures/?fwp_attributes=we
Spider dragline silke som torsionsaktuator drevet af fugt til applikationer som kunstig muskelI undersøgelsen, Liu et al. brugte dragline silke fra den afbildede edderkoppeart Nephila eduli, Nephila pilipes og Argiope versicolor. Billedkredit:Spider ID (spiderid.com/pictures/?fwp_attributes=we -
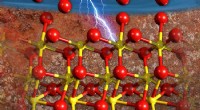 Atomer omarrangeres i elektrolyt og kontrollerer ionstrømmen under hårde forholdGrænsefladen mellem jernrig hæmatit (bund) og vand (øverst) ændres, efterhånden som overfladen bliver elektrisk ladet. Iltatomer (røde) omarrangerer sig på overfladen, udfylde alle steder, hvor der ma
Atomer omarrangeres i elektrolyt og kontrollerer ionstrømmen under hårde forholdGrænsefladen mellem jernrig hæmatit (bund) og vand (øverst) ændres, efterhånden som overfladen bliver elektrisk ladet. Iltatomer (røde) omarrangerer sig på overfladen, udfylde alle steder, hvor der ma
- Genteknologi afslører, hvordan giftige svampe koger giftstoffer op
- Sådan Find Age of a Lag af Rock, der er omgivet af lag af vulkansk Ash
- Qualcomm siger uber-hurtige 5G-netværk, telefoner, der kommer til USA inden april 2019
- Kan en stangmagnet lede elektricitet?
- Hvilke to fysikfejl opstår, når du ser og hører en fjern eksplosion på samme tid?
- Undersøgelse afslører, hvorfor timingen af fugletræk ændrer sig


